Карбонатная временная жесткость определяется по содержанию. Определение карбонатной жесткости воды. Жесткость воды, методы ее определения
О том, что такое "жесткость аквариумной воды, и в чем её выражают " мы уже писали. Но напомню вкратце, что жесткость подразделяют на постоянную и временную. Временная , она же карбонатная , она же устранимая жесткость связана с присутствием в воде наряду с катионами Ca 2+ и Mg 2+ гидрокарбонатных, или бикарбонатных анионов (HCO 3 - ) . При кипячении воды, гидрокарбонатные анионы вступают в реакцию с этими катионами и образуют с ними очень мало растворимые карбонатные соли, которые выпадают в осадок.
Твердость воды является традиционной мерой способности воды реагировать с мылом. Для жесткой воды требуется значительное количество мыла для получения пены, что также приводит к уменьшению количества труб горячей воды, котлов и других бытовых приборов. Жесткость воды вызвана растворенными поливалентными металлическими ионами. В пресных водах основными вызывающими твердость ионами являются кальций и магний; ионов стронция, железа, бария и марганца. Твердость может быть измерена реакцией поливалентных металлических ионов в образце воды с хелатирующим агентом, таким как этилендиаминтетрауксусная кислота, и обычно выражается как эквивалентная концентрация карбоната кальция. Твердость также может быть оценена путем определения концентраций отдельных компонентов твердости и выражения их суммы в терминах эквивалентного количества карбоната кальция.
Ca 2+ + 2HCO 3 - = CaCO 3 ↓ + H 2 O + CO 2
Временную жесткость можно устранить кипячением - отсюда и ее название. Аквариумисту невредно знать карбонатную жесткость воды в своих аквариумах. Это важный гидрохимический показатель, который часто приводится в справочной литературе, касающейся условий содержания и нереста рыб. Важно учитывать этот показатель и при выращивании многих аквариумных растений. Большинство аквариумистов уверенно, что с помощью продающихся в магазинах капельных тестов на карбонатную жесткость (КН) они определяют именно её. Но это забавное НЕДОРАЗУМЕНИЕ! Капельные тесты для аквариумистов-любителей, как в прочем и классический метод определения карбонатной жесткости путем титрования пробы воды соляной кислотой, измеряют вовсе не жесткость как таковую, то есть не концентрацию ионов кальция и магния, а щелочность - концентрацию в растворе гидрокарбонатных ионов . Гидрокарбонатные ионы могли оказаться в воде не только при растворении солей кальция и магния, поэтому судить о наличии ионов Ca 2+ и Mg 2+ по содержанию гидрокарбонатных ионов можно далеко не всегда. Но, обо всем по порядку…
Жесткость воды, методы ее определения
Степень твердости питьевой воды может быть классифицирована по концентрации ее карбоната кальция следующим образом: мягкая, от 0 до. Хотя твердость вызвана катионами, ее часто обсуждают в терминах карбонатной и некарбонатной жесткости. Твердость карбоната относится к количеству карбонатов и бикарбонатов, которые могут быть удалены или осаждены из раствора кипячением. Этот тип твердости отвечает за отложение окалины в трубах горячей воды и чайных чайниках. Некарбонатная жесткость обусловлена ассоциацией катионов, вызывающих твердость, с сульфатами, хлоридами и нитратами.
Если строго следовать определению карбонатной жесткости, то ее корректное измерение должно быть основано на кипячении заданного объема воды с последующим взвешиванием образовавшегося осадка (накипи). На практике это трудно выполнимо. Поэтому поступают иначе. Вот как определяют "карбонатную жесткость" с помощью общепринятой лабораторной методики.
Определение карбонатной жесткости воды проводится путем её титрования соляной кислотой. Титрование - это добавление в исследуемую пробу раствора реагента, концентрация которого заранее известна. По расходу этого реагента - он взаимодействует с тем веществом, содержание которого хотят определить, рассчитывают концентрацию определяемого вещества. В данном тесте принято пользоваться 0.05М раствором соляной кислоты (о том, что означает сокращение "М" можно прочитать ). Кроме этого, понадобится индикатор метиловый оранжевый
, который необходим для того, чтобы установить момент окончания титрования по резкому изменению цвета пробы. Для приготовления раствора индикатора небольшое его количество, 0.1 г растворяют в 100 мл дистиллированной воды. Точность здесь не требуется, можно все сделать на глазок.
Как правило, эти реактивы есть в любой химической лаборатории.
Он также упоминается как «постоянная твердость», потому что его нельзя удалить кипячением. Щелочность, показатель буферной способности воды, тесно связана с твердостью. По большей части щелочность образуется анионами или молекулярными видами слабых кислот, главным образом гидроксидом, бикарбонатом и карбонатом; другие виды, такие как бораты, фосфаты, силикаты и органические кислоты, также могут вносить небольшой вклад. Хотя многочисленные виды растворенных веществ могут способствовать щелочности воды, щелочность выражается в эквивалентном количестве карбоната кальция.
Проведение лабораторного теста на карбонатную жесткость:
Точно отмеряют 50 мл исследуемой воды. Добавляют несколько капель раствора метилового оранжевого, столько, чтобы окраска пробы получилось такой как в левом стаканчике на приведенном ниже рисунке:
При титровании в растворе произойдут следующие реакции:
Источники и уровни твердости
Поскольку щелочность большинства канадских поверхностных вод обусловлена наличием карбонатов и бикарбонатов, их щелочность близка к их твердости. Основными природными источниками твердости в воде являются осадочные породы, просачивание и сток из почв. В общем, твердые воды происходят в районах с толстыми слоями почвы и известняка. Грунтовые воды обычно сложнее поверхностных вод. Грунтовые воды, богатые углекислотой и растворенным кислородом, обычно обладают высокой сольватирующей способностью; в контакте с почвой или породами, содержащими значительное количество минералов, таких как кальцит, гипс и доломит, могут иметь место уровни твердости до нескольких тысяч миллиграммов на литр.
H + + HCO 3 - <-> H 2 CO 3 <-> CO 2 + H 2 O
Давайте сравним это и приведенное выше уравнение, которое показывало, что происходит с гидрокарбонатом кальция при кипячении. Как и при кипячении, конечными продуктами этих реакций являются вода и углекислый газ. Только вот кальций никак тут не участвует. Это и понятно, ведь ионы водорода, которые поступают в тестируемую воду при добавлении туда соляной кислоты, вступают в реакцию не с ионами кальция, а именно с гидрокарбонатными ионами.
Кислоту удобно набрать в шприц до отмеченного заранее деления и из него дозировано добавлять в раствор. Сначала порции кислоты могут быть относительно большими, но к концу титрования надо быть аккуратным и осторожным, цвет может поменяться буквально от одной капли. Способность тестируемой воды реагировать с ионами водорода по мере добавления кислоты будет постепенно уменьшаться и, наконец, окажется почти совсем исчерпанной - кончатся гидрокарбонатные ионы и последняя капля кислоты резко сместит в сторону кислых значений, так как связывать возникающие при ее диссоциации в воде ионы водорода уже будет "некому". При величине рН меньшей чем 4.3 гидрокарбонатных ионов в растворе уже нет (подробнее об этом рассказано ). Индикатор при этом значении рН изменит цвет раствора с желтого на оранжевый. Тут титрование надо будет прекратить. Титровать надо не торопясь, аккуратно перебалтывая воду в стаканчике. Лучше проделать эту процедуру несколько раз, точно засекая какой объем кислоты был израсходован. Затем вычислить СРЕДНИЙ ОБЪЕМ пошедшей на титрование кислоты. Зная этот объем рассчитывают карбонатную жесткость по формуле:
Двумя основными промышленными источниками твердости являются неорганическая химическая и горнодобывающая промышленность. Промышленные источники кальция и магния были кратко обсуждены в обзорах кальция и магния. Уровни твердости в Приморских провинциях не контролировались. В обзоре национального качества воды в качестве представителя канадских вод было выбрано 41 место.
Способы определения карбонатной жесткости воды
Эти города были в Онтарио и Саскачеване. Катионы, которые являются основными факторами, влияющими на твердость - кальций и магний, не являются непосредственной проблемой общественного здравоохранения. Эти параметры обсуждаются далее в отдельных обзорах.
Жесткость карбонатная (мг-экв/л) = (1000*С кислоты *V кислоты ):V воды
Где С кислоты - концентрация кислоты в молях (М/л), V кислоты - объем раствора кислоты использованный при титровании (мл), V воды - объем пробы воды, взятой для титрования (мл).
Если С кислоты = 0.05 М , а V воды = 50 мл , то
Жесткость карбонатная (мг-экв/л) = (1000*0.05*V кислоты ):50 = V кислоты
Ряд эпидемиологических исследований, в том числе в Канаде, Англия, Австралия и Соединенные Штаты, предположили, что существует обратная статистическая корреляция между жесткостью питьевой воды и некоторыми типами сердечно-сосудистых заболеваний. Другие работники, - сообщили, что существенные корреляции не могут быть продемонстрированы. Поэтому нельзя сделать никаких выводов.
Был проведен ряд других исследований, чтобы определить, существуют ли какие-либо связи между жесткостью питьевой воды и другими заболеваниями, включая рак., Опять же, обратные корреляции не было, но значение этих данных является дискуссионным. Внутреннее водоснабжение часто смягчается добавлением извести и кальцинированной соды или использованием ионообменной цеолитов. Умягчение воды может привести к добавлению в воду высоких уровней натрия, особенно в тех случаях, когда используются некоторые процессы ионного обмена.
То есть если вы титровали 50 мл воды 0.05 М соляной кислотой, то в этом случае карбонатная жесткость в мг-экв/л будет численно равна объему кислоты (в мл), израсходованному для титрования.
Например, если на титрование ушло 1.5 мл раствора кислоты, то карбонатная жесткость воды равна 1.5 мг-экв/л. Для перевода в градусы KH значение в мг-экв/л надо умножить на 2.804: 1.5*2.804=4.2°KH.
Хочу еще раз обратить ваше внимание на то, что описанный здесь метод анализа воды, обычно называют методом определения "карбонатной жесткости"
. На самом деле этим методом мы определили ЩЕЛОЧНОСТЬ воды
, то есть ее способность связывать ионы водорода, которые образуются при диссоциации в воде сильной кислоты. Покупные капельные тесты для аквариумной воды (KH-test, или тест на КН) также основаны на титровании воды кислотой и так же, как и описанный выше лабораторный тест, определяют щелочность. Надо полагать, что указанные в справочной литературе величины КН отражают не содержание в воде бикарбонатов кальция и магния, как об этом принято писать во всех аквариумных книжках, а именно щелочность, то есть любых бикарбонатов и других анионов, способных реагировать с ионами водорода. Хорошо это, или плохо? Скорее - хорошо. Для аквариумиста как раз важно знать насколько вода в его аквариуме способна противостоять закислению (нейтрализовывать поступающие в нее ионы водорода
). А сколько осадка такая вода даст на стенках труб в системе отопления, снизив при этом теплоотдачу, волнует его не сильно, если конечно он не теплотехник. Вспомним, что жесткость воды понятие не научное, а чисто утилитарное, но об этом уже было
написано ранее .
Хотя прямая связь между натрием и гипертонией не установлена у людей, считается целесообразным избегать ненужного добавления натрия в питьевую воду. Недавно рабочая группа Всемирной организации здравоохранения по проблемам потребления натрия в питьевой воде рекомендовала «не поощрять тенденции к излишнему потреблению натрия в водоснабжении». Поэтому рекомендуется, чтобы, когда считается, что смягчение воды путем ионного обмена является необходимым, отдельное несдержанное водоснабжение должно быть сохранено для питьевых и кулинарных целей.
Как мы уже отмечали, гидрокарбонатный ион может поступать в воду не только при растворении карбонатов кальция и магния, но и при растворении иных солей. Всем известная питьевая сода являет собой пример такого соединения: NaHCO 3 . Если внести питьевую соду в аквариум, то растворившись она даст ионы натрия и гидрокарбоната (о том, как растворяются соли в воде рассказано в статье о минерализации воды). Гидрокарбонатные ионы, как мы уже знаем, присоединяют к себе ионы водорода, поэтому вода в аквариуме от внесения питьевой соды становится менее кислой или приобретает щелочную реакцию - тут все зависит от дозы. Вот Вам и средство рН+! Питьевой содой и на самом деле пользуются многие аквариумисты. Небольшие ее добавки действительно застрахуют от неожиданных скачков рН. Решить достаточно соды внесено или нет можно измерив щелочность. Зная щелочность, вы можете оценить насколько вода в вашем аквариуме способна противостоять закислению - как говорят оценить БУФЕРНОСТЬ. Если щелочность пресной воды низкая (менее 1 мг-экв/л, или 2.804 о КН ), то и буферность ее невелика. Такая вода может резко скиснуть, например при пропуске очередной или при выключении аэрации на ночь. Интервал значений щелочности 1.2-1.8 мг-экв/л, или 3 - 5 о КН пригоден для большинства рыб и растений. Буферность воды при этом будет вполне достаточной для поддержания стабильной активной реакции воды - рН. Обычно щелочность аквариумной воды как раз и оказывается в указанном интервале или даже имеет еще большие значения - 2.5 мг-экв/л, или 7 о КН и выше (в этом случае возможны проблемы с выращиванием многих растений и нашествия водорослей). Но в регионах с мягкой слабокислой водой она может быть очень низкой. Так, в большинстве районов Петербурга водопроводная вода имеет щелочность 0.5 мг-экв/л. Поэтому многие любители африканских цихлид, для которых кислая вода - это нож острый, искусственно ее поднимают с помощью питьевой соды. Но! Если вы вносили в аквариум соду, чтобы поднять и стабилизировать рН, то вам не надо удивляться, если "карбонатная жесткость" вдруг превысит общую. Кстати, есть и природные воды с карбонатной жесткостью, превышающей общую, например, вода озера Танганьика. Этот результат может удивить, если не знать, что на самом деле определяет тест на карбонатную жесткость. Если вы вносили в воду аквариума NaHCO 3 , то есть не связанные с кальцием и магнием гидрокарбонатные ионы, то, естественно, их будет больше, чем ионов Са 2+ и Мg 2+ . Вот в этом и состоит суть парадокса, когда вполне логичная формула:
Смешивание с более мягкой водой
В районах с жесткой водой бытовые трубы могут забиваться с помощью шкалы; жесткие воды также вызывают инкрустации на кухонную утварь и увеличивают потребление мыла. Таким образом, жесткая вода является и неприятностью, и экономическим бременем для потребителя.
Одновременное определение общей некарбонатной и карбонатной жесткости воды с помощью прямой потенциометрии. Качество поверхностных вод в Канаде - обзор. Отдел качества воды, Управление внутренних вод. Химия для инженеров-сантехников. 2-е издание. Промышленные водные ресурсы Канады. Сфера применения, процедура и интерпретация обследований. Принцесса королевы, Оттава.
Общая жесткость = Постоянная жесткость + Временная жесткость
не выполняется из-за того, что временная больше общей
.
Понимание сути вещей порой позволяет творить чудеса, по крайней мере в глазах человека несведущего. Приносят нам как-то аквариумную воду на анализ. Надо мол разобраться рыбки всё дохнут и дохнут. На вопрос, измеряли ли рН? Нас заверили, что с рН совершенно точно все нормально. Ладно. Начали с измерения общей жесткости, потом карбонатную определили. Получилось, что карбонатная в несколько раз общую превосходит. Тут все уже ясно. Спрашиваем - зачем столько соды в аквариум насыпаете? Очень удивились, как мы про соду узнали. Оказывается добавление соды при каждой подмене воды - это де секретный и особо эффективный метод подсказанный по знакомству одним знатоком. Он, мол, гарантирует неизменно замечательный и оптимальный рН. Даже если чистить аквариумы редко, то вода не закиснет. Закиснуть-то она не закиснет. Но каково значение рН? Вы измеряли? Он же у вас больше 8 будет. А рыбки не только от кислой воды мрут . Нет отвечают, мы не измеряли. Сделали тест на рН. Он и в самом деле показал значение больше 8!
Определения и классификация естественно мягких и естественно жестких вод. Химические и физические характеристики воды в некоторых государствах-членах Европейского сообщества. В: Твердость питьевой воды и общественного здоровья. Труды Европейского научного коллоквиума, Люксембурга.
Качество потока в Аппалачии, связанное с дренажом угольных шахт, В: Качество воды в напряженной среде: показания в гидрологии окружающей среды. Национальный банк данных о качестве воды. Директорат по внутренним водам, Отдел качества воды, Окружающая среда Канады.
А Вы измеряете рН в своем аквариуме, или он у Вас и так "хороший"?
В. Ковалёв, Е. Ковалёва.
*
Здесь мы несколько упростили ситуацию. Все сказанное верно, если рН аквариумной воды 8.3 и ниже. Если же этот показатель выше значения 8.3, то в воде возможно присутствие не только гидрокарбонатов, но еще и карбонатов и даже гидроксидов щелочных металлов. В этом случае при добавлении кислоты в воду будут последовательно происходить следующие реакции:
OH -
+ H +
-> H 2
O
CO 3
2
-
+ H +
-> HCO 3
-
HCO 3
-
+ H +
Воды озера Гурон и озеро Верхнее. Доклад Международной совместной комиссии. Онтарио Министерство окружающей среды. Данные о качестве воды, озер и рек Онтарио. Отдел водных ресурсов. Связь между смертностью и жесткостью воды в Канаде. Краткое описание работы, системы водоснабжения Городская и частная секция, Отдел контроля загрязнения. Бюро эпидемиологии, здравоохранения и социального обеспечения Канады.
Ишемическая болезнь сердца, жесткость воды и миокардиальный магний. Внезапная смерть и ишемическая болезнь сердца. Распространенность и патологические изменения ишемической болезни сердца в жесткой воде и в области мягкой воды. Твердость водоснабжения и сердечно-сосудистых заболеваний. К. цитируется в справочнике. Жесткость воды и сердечно-сосудистые заболевания.

8 Лабораторная работа №16
Жесткость воды, методы ее определения
Цель работы: познакомиться с понятием жесткости воды; овладеть методиками определения общей, временной (карбонатной) и постоянной (некарбонатной) жесткости воды методами потенциометрического и кислотно-основного титрования.
Твердость питьевой воды и сердечно-сосудистых заболеваний. Соотношение качества питьевой воды и сосудистых заболеваний. Эпидемиологическое исследование внезапной смерти в труднодоступных и мягких акваториях. Смертность и жесткость местных водоснабжения.
Клинические и биохимические показатели среди мужчин, живущих в труднодоступных и мягких акваториях. Записи о потреблении воды в Брисбене и сезонности при местной смерти. Связь между смертностью от сердечно-сосудистых заболеваний и обработанной водой. Изменение в штатах и 163 крупнейших муниципалитетах.
Оборудование и реактивы: 0,1н. соляная кислота; 0,1н. раствор трилона Б; индикаторы: эриохром черный кристаллический, фенолфталеин, метиловый оранжевый; аммиачный буфер; рН-метр; магнитная мешалка; бюретки; пипетки на 100 мл или мерные цилиндры; колбы на 250 мл и 500 мл; стаканы на 200 – 250 мл; мерные колбы на 200 мл; бумажные фильтры.
8.1 Теоретические пояснения
Муниципальная питьевая вода и смертность от сердечно-сосудистых заболеваний. Минералы в городской воде и атеросклеротическая сердечная смерть. Взаимосвязь между содержанием микроэлементов питьевой воды и хроническими заболеваниями, наблюдаемым влиянием микроэлементов в питьевой воде на здоровье человека.
Здоровье и экономические аспекты жесткости воды и коррозионной активности. Смертность и жесткость воды в трех сопоставленных сообществах в Лос-Анджелесе. Фатальная артериосклеротическая болезнь сердца, жесткость воды у себя дома и социально-экономические характеристики.
Природная вода в своем составе всегда содержит различные примеси: соли и газы, механические примеси, находящиеся во взвешенном состоянии, эмульсии, гидрозоли и другие образования. Некоторые соли, присутствующие в воде, вызывают ее жесткость.
Жесткость воды – это совокупность свойств воды, обусловленных присутствием в ней катионов Ca 2+ и Mg 2+ , реже Fe 2+ .
Объяснение вариаций смертности от сердечно-сосудистых заболеваний в районе мягкой воды. Водные составляющие и микроэлементы в связи с сердечно-сосудистыми заболеваниями. Проблемы, связанные с металлами в питьевой воде. Обзор и последствия текущих и прогнозируемых исследований за пределами европейских сообществ.
Твердость карбоната или временная твердость
Контроль коррозии питьевой воды. Потенциальные аспекты общественного здравоохранения в отношении микроэлементов и качества питьевой воды. Цели качества питьевой воды.
Некарбонатная или постоянная твердость
Таблица преобразования единицы твердости. Классификация жесткости воды. Большинство котельных установок имеют размягченную или деминерализованную воду для макияжа. Поэтому необходимы хорошие программы внутреннего лечения. Чтобы понять вашу воду, вам нужно получить копию ежегодного анализа воды в вашем районе.В жесткой воде ухудшается пенообразование и увеличивается расход мыла при стирке, так как часть содержащихся в нем растворимых солей жирных кислот переходит в нерастворимое состояние:
2C 17 H 35 COONa + CaSO 4 = (C 17 H 35 COO) 2 Ca + Na 2 SO 4 .
При этом также ухудшается качество тканей вследствие осаждения на них нерастворимых кальциевых и магниевых солей высших жирных кислот.
Позвоните в отдел общественных работ в мэрии и попросите копию, они обычно отправят вам одну бесплатную версию. Отчеты о качестве воды в основном ориентированы на законы о безопасной питьевой воде, касающиеся загрязнений, таких как пестициды, бактерии и токсичные металлы.
В качестве пивоваров нас интересуют вторичные или эстетические стандарты, которые имеют отношение к вкусу и рН. При оценке пивоваренной воды необходимо учитывать несколько важных ионов. Основными ионами являются кальций, магний, бикарбонат и сульфат. Натрий, хлорид и сульфат могут влиять на вкус воды и пива, но не влияют на рН затора, как и другие. Концентрации ионов в воде обычно обсуждаются как части на миллион, что эквивалентно миллиграмму вещества на литр воды. Описания этих ионов следуют за докладом о воде.
В воде с повышенной жесткостью плохо развариваются овощи и мясо, так как катионы кальция образуют с белками нерастворимые соединения. Большая магниевая жесткость придает воде горький вкус.
Жесткость воды хозяйственно-питьевых водопроводов не должна превышать 7 ммоль экв./л . По величине жесткости воду условно подразделяют на мягкую (до 4 ммоль экв./л ), средней жесткости (4 – 8 ммоль экв./л ), жесткую (8 – 12 ммоль экв./л ) и очень жесткую (более 12 ммоль экв./л ).
Таблица 12 - Отчет по качеству воды в столице штата Лос-Анджелес. Кальций является основным ионом, который определяет жесткость воды и имеет 2 заряда. Как и в наших собственных телах, кальций играет важную роль во многих дрожжевых, ферментных и белковых реакциях, как в пюре, так и в кипячении. Это способствует ясности, вкусу и стабильности в готовом пиве. Добавки кальция могут потребоваться для обеспечения достаточной активности фермента для некоторых сливок в воде с низким содержанием кальция. Кальций, который сочетается с бикарбонатами в воде, называется «временная твердость».
Общая жесткость складывается из карбонатной (временной) и некарбонатной (постоянной). Карбонатная жесткость обусловлена присутствием в воде гидрокарбонатов кальция, магния, а иногда также и гидрокарбоната железа (II). Этот вид жесткости можно устранить кипячением:
Ca (HCO 3 ) 2 CaCO 3 + H 2 O + CO 2
Mg(HCO
3
)
2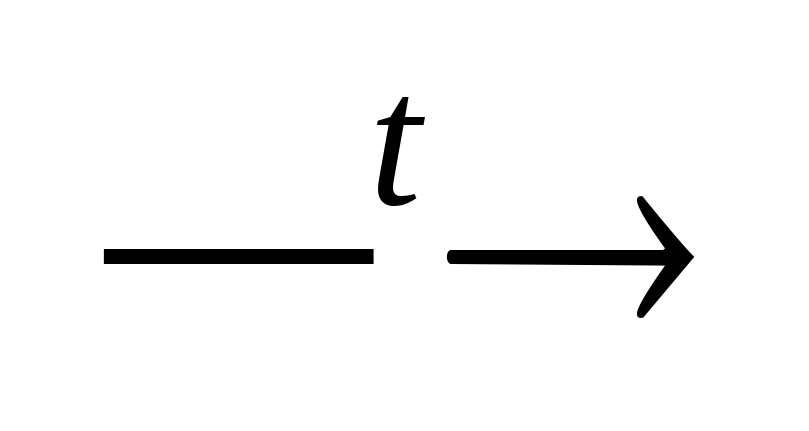 MgCO
3
+ H
2
O
+ CO
2
;
MgCO
3
+ H
2
O
+ CO
2
;
2MgCO
3
+ H
2
O
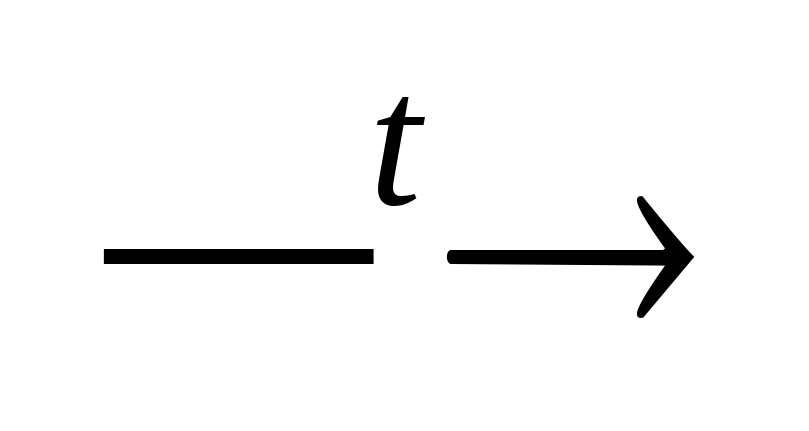 (MgOH)
2
CO
3
+ CO
2
(MgOH)
2
CO
3
+ CO
2
(MgOH)
2
CO
3
+H
2
O
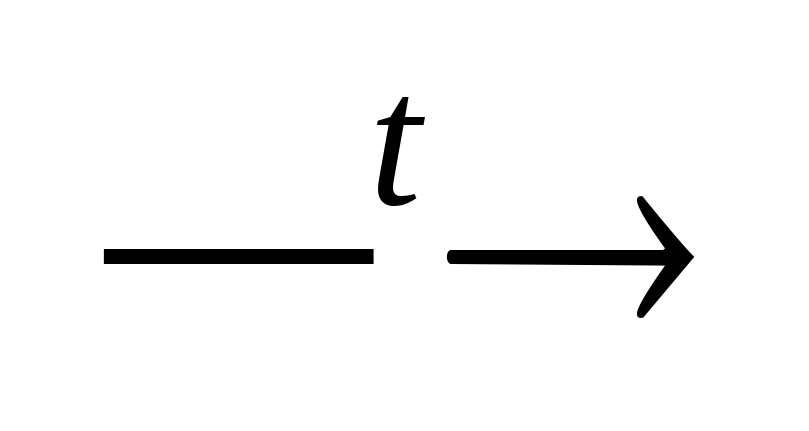 2Mg(OH)
2
+CO
2
2Mg(OH)
2
+CO
2
Fe(HCO
3
)
2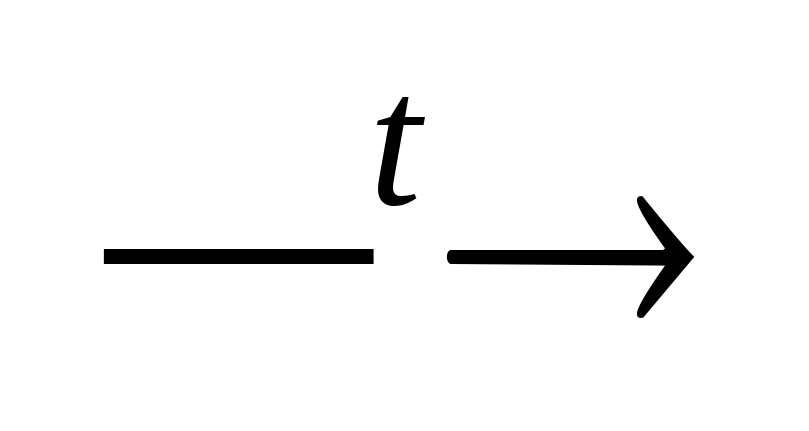 Fe(OH)
2
+ 2CO
2
;
Fe(OH)
2
+ 2CO
2
;
4Fe(OH) 2 + O 2 + 2 H 2 O 4Fe(OH) 3 .
При кипячении воды растворенные в ней гидрокарбонаты разлагаются, и карбонатная жесткость сильно снижается, однако полного устранения карбонатной жесткости не происходит вследствие того, что карбонаты кальция и магния несколько растворим в воде.
Наряду с понятием карбонатная жесткость, используется термин устранимая жесткость. Это та величина, на которую понижается жесткость при десятиминутном кипячении воды. Жесткость, оставшаяся после кипячения воды, называется постоянной жесткостью.
Для уменьшения карбонатной жесткости применяют также метод известкования:
Ca(HCO 3 ) 2 + Ca(OH) 2 2CaCO 3 + 2H 2 O
Mg(HCO 3 ) 2 + 2Ca(OH) 2 Mg(OH) 2 + 2CaCO 3 + 2H 2 O.
Некарбонатная жесткость обусловлена присутствием в воде растворимых, устойчивых к нагреванию солей кальция и магния. Чаще всего это сульфаты и хлориды.
Некарбонатную жесткость можно устранить обработкой воды карбонатом или фосфатом натрия:
MeSO 4 + Na 2 CO 3 MeCO 3 + Na 2 SO 4 .
Для устранения жесткости применяют также катиониты. Это ионообменные смолы и алюмосиликаты, содержащие в своем составе подвижные катионы, например, Na + , H + , способные обмениваться на катионы среды. Если пропускать воду через слои катионита, то его подвижные катионы будут обмениваться на катионы кальция и магния, при этом катионы жесткости остаются в катионите, а подвижные ионы катионита переходят в раствор. При помощи Н + -катионирования умягчают воду с преобладанием карбонатной жесткости, а при помощи Na + -катионирования – с преобладанием некарбонатной жесткости.
Для умягчения воды можно также использовать и физические методы: электродиализ, ультразвуковую, магнитную и магнитно-ионизационную обработку воды.
Жесткость воды определяется аналитически.
Карбонатную (устранимую или временную) жесткость воды определяют титрованием воды соляной кислотой:
Са(НСО 3 ) 2 + 2НС1 = CaCI 2 + 2 H 2 O + 2С O 2
Mg (HCO 3 ) 2 + 2НС1 = MgCl 2 + 2Н 2 О + 2СО 2
Точку эквивалентности можно определить либо потенциометрическим титрованием с помощью рН-метра (определение объема раствора соляной кислоты в точке скачка рН), либо титрованием в присутствии кислотно-основных индикаторов (чаще всего метилового оранжевого).
Для выбора соответствующего кислотно-основного индикатора необходимо построить интегральную кривую титрования на основании данных потенциометрического титрования, а затем выбрать такой индикатор, интервал перехода окраски которого попадает в область скачка рН на кривой титрования. В таблице 8.1 приводятся интервалы перехода окраски для некоторых индикаторов.
Таблица 8.1 – Характеристики наиболее часто применяемых кислотно-основных индикаторов
|
Индикатор |
Интервал перехода окраски, единицы рН |
Изменение окраски раствора при возрастании рН |
|
|
О-крезоловый синий |
красная ® желтая |
||
|
Тимоловый синий |
красная ® желтая |
||
|
Метиловый оранжевый |
красная ® оранжевая |
||
|
Бромкрезоловый зеленый |
желтая ® синяя |
||
|
Бромметиловый зеленый |
желтая ® синяя |
||
|
красна ® синяя |
|||
|
Бромтимоловый синий |
желтая ® синяя |
||
|
Феноловый красный |
желтая ® красная |
||
|
Фенолфталеин |
бесцветная ® малиновая |
||
|
Ализариновый желтый |
бледно-лимонная ® желтая |
Некарбонатную (постоянную) жесткость воды определяют методом обратного титрования. К отмеренному объему исследуемой воды добавляют определенный объем раствора карбоната натрия известной концентрации и выпаривают раствор досуха. При этом образуются нерастворимые в воде карбонаты кальция и магния.
Са 2+ + Mg 2+ + 2Na 2 CO 3 = CaCO 3 + MgCO 3 + 2Na +
Сухой остаток, представляющий из себя смесь карбонатов кальция, магния, натрия и других солей натрия, растворяют в не содержащей СО 2 воде, отфильтровывают нерастворимые в воде карбонаты кальция и магния и титриметрическим способом определяют в растворе количество избыточного Na 2 CO 3 , не вошедшего в реакцию осаждения карбонатов. Специальными опытами показано, что при этом Na 2 CO 3 не реагирует с гидрокарбонатами кальция и магния. Именно поэтому, рассмотренный метод позволяет определять постоянную жесткость воды.
Современным методом определения общей жесткости воды является титрование воды раствором трилона Б в присутствии специальных индикаторов-хромогенов, чаще всего эриохрома черного. Титрование проводится в аммиачной среде при значении рН раствора в пределах 9-10.
Трилон Б (комплексон III) – это динатриевая соль этилендиамминтетрауксусной кислоты (NaO 2 CCH 2 ) 2 N(CH 2 ) 2 N(CH 2 CO 2 H) 2 , сокращенно – Na 2 H 2 ЭДТА .
Na 2 H 2 ЭДТА + Са 2+ (или Mg 2+ ) ® Na 2 Ca ЭДТА + 2H + .
Хромоген образует с ионами магния и другими ионами относительно непрочные комплексные соединения, окрашенные в красно-фиолетовый цвет. При титровании трилоном Б содержащиеся в воде ионы Са 2+ и Mg 2+ , а также ионы Cu 2+ , Zn 2+ , Mn 2+ , Cd 2+ , Ni 2+ , Al 3+ , Fе 2+ , Fe 3+ реагируют с ним и образуют мало диссоциированные бесцветные прочные комплексные соединения. В конце титрования ионы магния, кальция и другие переходят от комплексного соединения с хромогеном к трилону Б, с образованием прочных бесцветных комплексов.
Поэтому в точке эквивалентности красно-фиолетовая окраска раствора исчезает. Однако раствор не обесцвечивается, а окрашивается в сине-фиолетовый цвет – цвет самого хромогена эриохрома черного при рН = 9-10 (аммиачный буфер). Это указывает на окончание титрования.
Так как трилон Б образует прочные комплексы со всеми катионами кальция и магния вне зависимости от характера аниона, то комплексонометрическим методом определяют именно общую жесткость воды.
Проба воды должна характеризовать действительный ее состав, поэтому при отборе пробы из водопровода воду спускают в течение 10-15 минут. Когда склянка наполнится, воду некоторое время переливают через край.
Из рек и ручьев отбирают пробы воды на глубине 0,75 м в нескольких местах, около берегов и в середине реки. Отдельные пробы смешивают вместе. Анализ воды проводят сразу же после взятия пробы или, в крайнем случае, при соответствующем хранении спустя несколько часов.
8.2 Методика проведения опытов
8.2.1 Опыт №1. Определение карбонатной жесткости воды
Мерным цилиндром отбирают в две конические колбы по 100 мл исследуемой воды из-под крана. Оттитровывают воду в первой колбе 0,1н. раствором НСl. Для этого с помощью рН-метра фиксируют значения рН воды после каждого прибавления очередной порции HCl из бюретки. Объем каждой порции HCl составляет 0,5 мл.
По полученным значениям рН и объема прилитой кислоты строят интегральную и дифференциальную кривые титрования. Из кривых титрования определяют точку эквивалентности. Пользуясь данными таблицы 8.1 выбирают индикатор для экспресс-анализа. Интервал перехода окраски выбранного индикатора должен находиться в пределах скачка рН на интегральной кривой титрования.
Карбонатную жесткость воды Ж карб. , выраженную в ммоль экв./л , определяют по формуле (8.1):
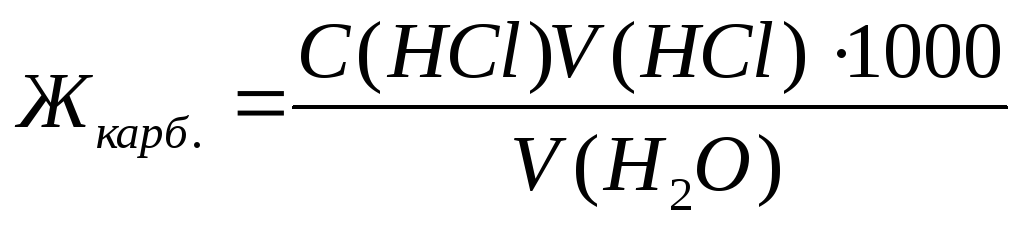 , (8.1)
, (8.1)
где V (HCl ) – объем раствора 0,1н. НСl, израсходованного до достижения точки эквивалентности, мл ;
С(HCl ) – концентрация раствора HCl, моль экв./л ;
V (Н 2 О) – объем исследуемой воды, мл ;
моль к ммоль .
Затем проводят титрование воды во второй колбе 0,1н. раствором НСl. Только на этот раз за ходом титрования следят визуально, по изменению окраски выбранного индикатора. Вблизи точки эквивалентности последняя капля титранта вызывает резкое изменение окраски раствора, содержащего индикатор. Фиксируют объем прибавленной кислоты к моменту достижения точки эквивалентности. Проводят расчет карбонатной жесткости воды по формуле (8.1)
8.2.2 Опыт №2. Определение общей жесткости воды
В коническую колбу отмеряют пипеткой 100 – 150 мл исследуемой воды, добавляют 5 мл аммиачного буфера и несколько кристаллов эриохрома черного до образования заметной вишнево-красной окраски. При слабой окраске раствора проверяют его рН универсальной индикаторной бумагой. Значение рН должно находиться в интервале 8-11. При необходимости корректируют рН добавлением в раствор буферной смеси.
Раствор оттитровывают стандартным раствором трилона Б до точки резкого перехода вишнево-красной окраски в синюю. Окраска раствора от избытка трилона Б остается неизменной, поэтому в конце титрования рабочий раствор трилона Б прибавляют осторожно, по каплям, энергично перемешивая.
Титрование повторить два раза и взять среднее значение объема израсходованного раствора трилона Б.
Общую жесткость воды Ж общ. , выраженную в ммоль экв./л , определяют по формуле (8.2):
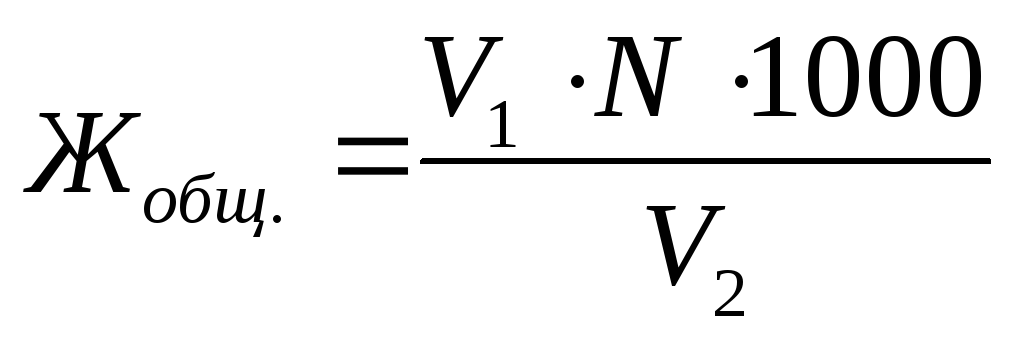 , (8.2)
, (8.2)
где V 1 – объем рабочего раствора трилона Б, израсходованного на титрование пробы воды, мл ;
N – молярная концентрация эквивалента рабочего раствора трилона Б, моль экв./л ;
V 2 – объем исследуемой воды, мл ;
1000 – коэффициент пересчета от моль к ммоль .
По разности значений общей и карбонатной жёсткости определить постоянную жесткость. Сделать вывод о характере и степени жесткости исследуемой воды.
8.3 Примеры решения задач
Пример 1
Рассчитайте общую жесткость воды (ммоль экв./л ), если в 0,15 л воды содержится 16,2 мг гидрокарбоната кальция, 2,92 мг гидрокарбоната магния, 11,10 мг хлорида кальция и 9,50 мг хлорида магния.
Решение
Выразим общую жесткость воды как сумму миллимолярных концентраций эквивалентов двухзарядных катионов металлов (или соответствующих им солей) в воде:
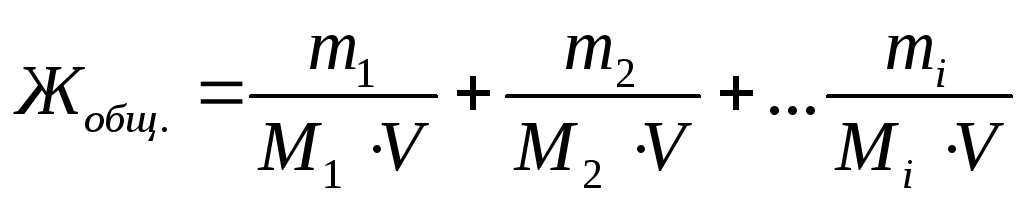 ,
,
где m 1 , m 2 , m i – массы двухзарядных катионов металлов, либо массы соответствующих им солей, либо массы веществ, пошедших на устранение жесткости воды, мг ;
M 1 , M 2 , M i – молярные массы эквивалентов двухзарядных катионов металлов, либо массы соответствующих им солей, либо массы веществ, пошедших на устранение жесткости воды, г/моль ;
V – объем воды, л .
Молярные массы эквивалентов солей, перечисленных в условии задачи, рассчитываются по формуле:
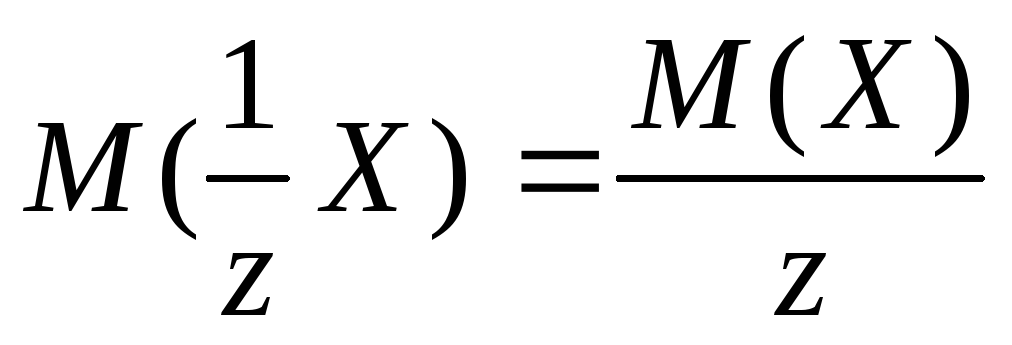 ,
,
где z – эквивалентное число, для солей жесткости оно равно 2;
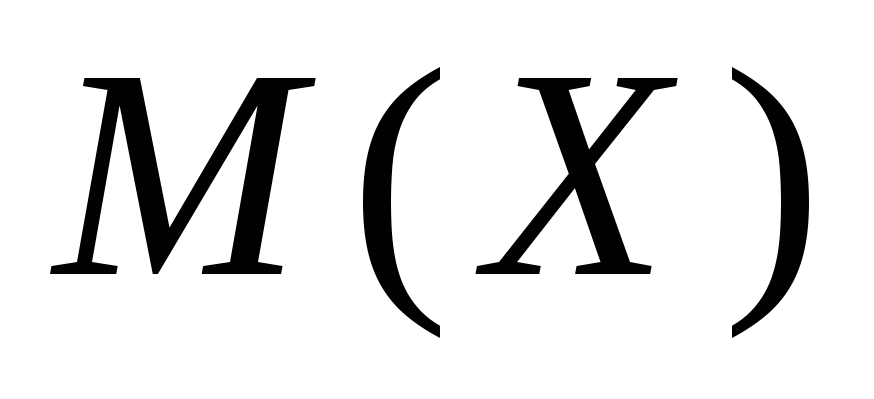 –молярная масса
соли Х
.
–молярная масса
соли Х
.
Общая жесткость данного образца воды равна сумме временной и постоянной жесткости:
2,56 ммоль экв./л
Пример 2
Определите временную жесткость воды, если на титрование 0,1 л воды, содержащей гидрокарбонат магния, израсходовано 7,2∙10 -3 л 0,14н . раствора HCl .
Решение
При титровании воды соляной кислотой происходит реакция:
Mg (HCO 3 ) 2 + 2НС1 = MgCl 2 + 2Н 2 О + 2СО 2
Временную жесткость воды рассчитаем по формуле (8.1):
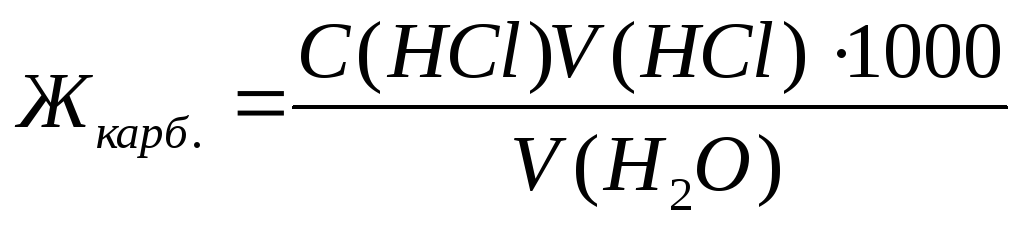
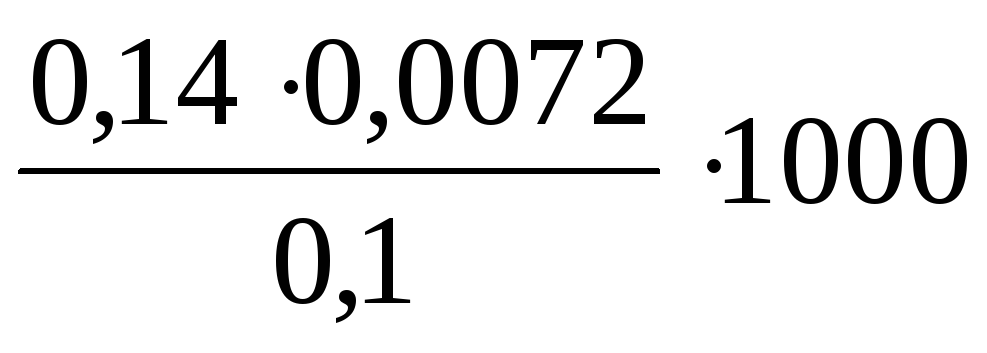 =10,08 ммоль
экв./л
=10,08 ммоль
экв./л
Пример 3
Для устранения общей жесткости по известково-содовому методу добавлено 7,4 г Са(ОН) 2 и 5,3 г Na 2 CO 3 . Рассчитать временную и постоянную жесткость воды.
Решение
Добавление к воде Са(ОН) 2 может устранить временную жесткость, а добавление Na 2 CO 3 – постоянную жесткость. При добавлении этих реагентов к воде происходят следующие реакции:
Ca(HCO 3 ) 2 + Ca(OH) 2 2CaCO 3 + 2H 2 O
Mg(HCO 3 ) 2 + 2Ca(OH) 2 Mg(OH) 2 + 2CaCO 3 + 2H 2 O.
Ca(N О 3 ) 2 + Na 2 CO 3 = MeCO 3 + 2NaNO 3
Mg(N О 3 ) 2 + Na 2 CO 3 = MeCO 3 + 2NaNO 3
Временную жесткость воды Ж вр измеряют количеством вещества эквивалентов гидроксида кальция, участвующего в реакции, а постоянную жесткость Ж пост – количеством вещества эквивалентов карбоната натрия.
M (1/2Са(ОН) 2 ) = 74/2=37 г/моль ;
M (1/2 Na 2 CO 3 ) = 106/2=53 г/моль ;
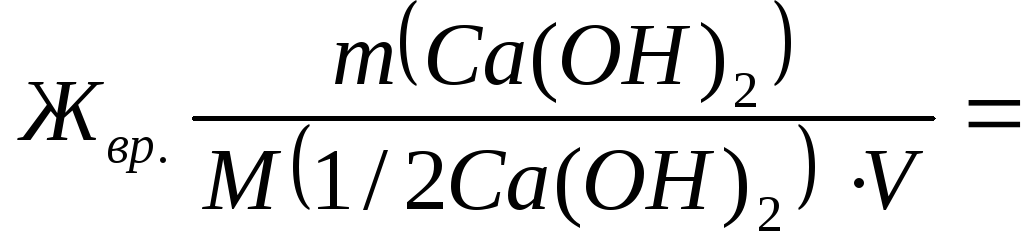 7400/(37∙50) = 4 ммоль
экв./л
;
7400/(37∙50) = 4 ммоль
экв./л
;
![]() 5300/(53∙50)
= 2 ммоль
экв./л
5300/(53∙50)
= 2 ммоль
экв./л
Общая жесткость воды равна:
Ж общ = Ж вр + Ж пост = 4 + 2 = 6 ммоль экв./л
8.4 Требования к уровню подготовки студентов
Знать понятия: общая, временная (карбонатная) и постоянная (некарбонатная) жесткость воды.
Понимать для чего необходимо умягчение воды.
Иметь представление о методах устранения временной и постоянной жесткости.
Уметь производить расчеты жесткости воды, а также количеств реактивов, необходимых для ее устранения.
8.5 Задания для самоконтроля
При определении карбонатной жесткости воды используют индикатор метиловый оранжевый. Почему нельзя использовать фенолфталеин?
Почему при кипячении воды ее временная (устранимая) жесткость уменьшается?
Почему комплексонометрическим методом определяют только общую жесткость?
Какие соли вызывают постоянную жесткость? Почему она так называется?
Что происходит при кипячении жесткой воды с гидроксидом натрия? Почему израсходованное количество NaOH эквивалентно суммарному количеству растворенных солей некарбонатного происхождения?
Что такое обратное титрование и как его осуществляют? Какие преимущества имеет этот метод?
Какой вид жесткости воды определяют при помощи титрования раствором кислоты? Какая реакция при этом происходит?
Какая характеристика раствора изменяется при кислотно-основном титровании? Какими методами можно фиксировать точку эквивалентности?
Благодаря каким свойствам трилон Б (комплексон III) можно использовать в качестве титранта при определении общей жесткости воды?
Для чего используется аммиачный буферный раствор при определении общей жесткости?
Почему при определении общей жесткости воды прибавление кристаллов эриохрома черного вызывает покраснение раствора, а в точке эквивалентности раствор синеет?
На титрование 100 мл воды пошло 2 мл 0,1н . раствора трилона Б. Рассчитайте жесткость воды.
Вода содержит в 10 л 0,95 г хлорида магния и 1,62 г гидрокарбоната кальция. Определить карбонатную, некарбонатную (постоянную) и общую жесткость этого образца воды.
Чему равна жесткость воды, выраженная в ммоль экв./л , если концентрация СаCl 2 составляет 0,005 моль/л?
Растворимость СаSO 4 в воде 0,202%. Вычислите жесткость насыщенного раствора этой соли, принимая его плотность за 1,0 г/мл .
Для умягчения 100 л воды потребовалось 12,72 г Na 2 CO 3 . Чему равна жесткость образца воды в ммоль экв./л ?
На титрование 0,05 л образца воды израсходовано 4,8∙10 -3 л 0,1н . раствора HCl . Чему равна карбонатная жесткость воды?
Какую массу гашеной извести надо прибавить к 2,5 л воды, чтобы устранить ее временную жесткость, равную 4,43 ммоль экв./л ?
При определении временной жесткости на титрование 0,1 л воды израсходовано 5,25∙10 -3 л 0,101н . раствора HCl . Какова величина жесткость этой воды?
Образец воды объемом 1 литр содержит 48,6 мг гидрокарбоната кальция и 29,6 мг сульфата магния. Какое количество Са 2 + и Mg 2 + содержится в литре этой воды? Чему равна общая, постоянная и карбонатная жесткость воды?
Некарбонатная жесткость воды равна 3,18 ммоль экв./л . Какую массу Na 3 Р O 4 надо взять, чтобы умягчить 1м 3 воды?
8.6.1 Глинка Н.Л. Общая химия: Учебное пособие для вузов/ Под ред. А.И.Ермакова. – М.: Интеграл-Пресс, 2010. – 728 с.
8.6.2 Романцева Л.М. Сборник задач и упражнений по общей химии/ Л.М.Романцева, З.Л.Лещинская, В.А.Суханова. – М.: Высш. шк., 1991. – С.146 – 149.










