Електролиза. Електролиза на стопилки и електролитни разтвори Получаване на солна киселина чрез електролиза
ЕЛЕКТРОЛИЗА
стопилки и разтвори на електролити
чрез електролиза нарича набор от химични реакции, които се случват по време на преминаването на постоянен ток чрез електрохимична система, състояща се от два електрода и електролитна стопилка или разтвор.
Химическата същност на електролизата се състои в това, че това е окислително-възстановителна реакция, протичаща под въздействието на постоянен електрически ток, като процесите на окисление и редукция са пространствено разделени.
Катод - електрод, върху който се редуцират катиони или вода. Заредена е отрицателно.
Анод - електрод, върху който се окисляват аниони или вода. Заредена е положително.
1. Електролиза на стопилки на соли, основи.
По време на електролизата на стопилките металните катиони винаги се редуцират на катода.
K(-): Men+ + nē → Me0
Анодният процес се определя от състава на аниона:
а) Ако анионът на безкислородна киселина (Cl-, Br-, I-, S2-), тогава този анион претърпява анодно окисление и се образува просто вещество:
A(+): 2Cl - - 2ē → Cl2 или A(+): S2- - 2ē → S0
б) Ако кислородсъдържащ анион (SO42-, SiO32-, HO- и т.н.) се подложи на анодно окисляване, тогава неметалът образува оксид (без да променя степента си на окисление) и се освобождава кислород.
A(+): 2SiO32-- 4ē → 2SiO2 + О2
A(+): 2SO32-- 4ē → 2SO2 + O2
A(+): 4РO43-- 12ē → 2Р2O5 + 3О2
A(+): 4NO3-- 4ē → 2N2O5 + О2
A(+): 4HO-- 4ē → 2H2O + O2
Пример 1.1. Разтопена сол ZnCl2
ZnCl2 Û Zn2+ + 2Cl-
S: ZnCl2 електролиза на Zn + Cl2
Пример 1.2. Алкална стопилка NaOH
NaOH Û Na+ + OH-
Общото уравнение на електролизата се получава чрез събиране на дясната и лявата част на уравненията, при условие че електроните, участващи в катодните и анодните процеси, са равни.
https://pandia.ru/text/80/299/images/image006_58.gif" width="70" height="12">4 Na+ + 4 ē + 4 OH - - 4 ē електролиза 4 Na0 + O2 + 2H2O
4 Na+ + 4 OH - електролиза 4 Na0 + O2 + 2H2O - йонно уравнение
4NaOH електролиза 4Na + 2H2O + O2 - молекулно уравнение
Пример 1.3. Разтопена сол Na2SO4
Na2SO4 Û 2Na+ + SO42-
K(-): Na+ + 1 ē Þ Nao *4
A(+): 2SO42- - 4 ē Þ O2 + 2SO3
4Na+ +2SO42- Þ 2Nao + O2 + 2SO3 – уравнение на йонна електролиза
2Na2SO4 електролиза 4Nao + O2 + 2SO3 - молекулно уравнение
К А
Пример 1.4. Разтопена сол AgNO3
AgNO3 Û Ag+ + NO3-
K(-): Ag+ + 1 ē Þ Ago *4
A(+): 4NO3- - 4 ē Þ 2N2O5 + 2O2 *1
4Ag+ + 4NO3- електролиза 4Ag + 2N2O5 + 2O2
4AgNO3 електролиза 4Ag + 2N2O5 +2O2
К А
Задачи за самостоятелна работа . Съставете уравнения за електролиза на стопилки на следните соли: AlCl3, Cr2(SO4)3, Na2SiO3, K2CO3.
2. Електролиза на разтвори на соли, хидроксиди и киселини.
Електролизата на водни разтвори се усложнява от факта, че водата може да участва в процесите на окисление и редукция.
катодни процеси определя се от електрохимичната активност на солния катион. Колкото по-вляво е металът в серията на напрежението, толкова по-трудно е неговите катиони да бъдат редуцирани на катода:
![]() Ли
К
ок
Na
мг
Ал
Мн
Zn
Кр
Те
Ni
сн
Pb
H2
Cu
hg
Ag
Пт
Au
Ли
К
ок
Na
мг
Ал
Мн
Zn
Кр
Те
Ni
сн
Pb
H2
Cu
hg
Ag
Пт
Au
аз групаIIгрупаIIIгрупа
За метални катиони до Al включително (група I), катодният процес е редукция на водород от вода:
(-)K: 2H2O + 2ē → H2 + 2HO-
За металните катиони след водорода (група III) катодният процес е тяхното редуциране до метал:
(-) K: Men+ + nē → Me0
За метални катиони в серията напрежения от Mn до H2 (група II) съществуват паралелни конкурентни процеси за редукция на метални катиони и водород от вода:
(-) K: Men+ + nē → Me0
2Н2О + 2ē → Н2+ 2НО-
Кой от тези процеси ще надделее зависи от редица фактори: Me активност, pH на разтвора, концентрация на сол, приложено напрежение и условия на електролиза.
Анодни процеси се определят от състава на солните аниони:
а) Ако анионът е безкислородна киселина (Cl-, Br-, I-, S2- и т.н.), тогава той се окислява до прости вещества (с изключение на F-):
A(+): S2- - 2ē → S0
б) В присъствието на съдържащ кислород анион (SO42-, CO32- и т.н. или OH-), само водата претърпява анодно окисление:
A(+): 2H2O - 4ē → O2 + 4H+
Помислете за примери, илюстриращи всички възможни опции:
Пример 2.1 . разтвор на KCl сол
K(-): 2H2O + 2e - Þ H2 + 2OH-
A(+): 2Cl - - 2e - Þ Cl2
å: 2H2O + 2Cl - електролиза H2 + 2OH - + Cl2 - уравнение на йонна електролиза
2KCl + 2H2O електролиза H2 + 2KOH + Cl2 - електролиза молекулярно уравнение
К А
Пример 2.2 . Разтвор на сол CuCl2
CuCl2 Û Cu2+ + 2Cl-
K(-): Cu2+ + 2e - Þ Cuo
A(+): 2Cl- -2e - Þ Cl2
å: CuCl2 електролиза на Cu + Cl2
Пример 2.3. Разтвор на сол FeCl2
FeCl2 Û Fe2+ + 2Cl-
Желязото принадлежи към металите от група II, така че на катода ще протичат два паралелни процеса:
1-ви процес:
(-) K: Fe2+ + 2ē → Fe0
(+)A: 2Cl - - 2ē → Cl2
Fe2+ + 2Cl - el-z Fe0 + Cl2 - йонно уравнение на процеса
FeCl2 el-z Fe0 + Cl2 - молекулно уравнение на процеса
2-ри процес:
(-)K: 2H2O + 2ē → H2+ 2OH-
(+)A: 2Cl - - 2ē → Cl2
2H2O + 2Cl - → H2+ 2OH - + Cl2 - йонно уравнение на процеса
2H2O + FeCl2 електролиза на H2 + Fe(OH)2 + Cl2 - молекулно уравнение.
По този начин, в катодното пространство Fe, H2 и Fe(OH)2 ще се образуват в различни съотношения в зависимост от условията на електролиза.
Пример 2.4 . Разтвор на сол Na2SO4.
Na2SO4 Û 2Na+ + SO42-
K(-) 2H2O + 2e - Þ H2 + 2OH - *2
A(+) 2H2O – 4e - Þ O2 + 4H+
å: 6H2O електролиза 2H2 + 4OH - + O2 + 4H+
å: 6H2O + 2Na2SO4 електролиза 2H2 + 4 NaOH + O2 + 2H2SO4
в катодното пространство в анодното пространство
Когато електрическият ток е изключен и съдържанието на катодното и анодното пространство се смеси, крайният резултат от електролизата може да бъде представен по схемата:
2H2O el-z 2H2 + O2,
тъй като алкалът ще реагира с киселината, за да образува 2 mol сол и 4 mol вода.
Пример 2.5 . Електролиза на разтвор на CuSO4.
CuSO4 Û Cu2+ + SO42-
K(-): Cu2+ + 2e - Þ Cuo
A(+): 2H2O – 4e - Þ O2 + 4H+
å: 2Cu2+ + 2H2O електролиза 2Cuo + O2 + 4H+
å: CuSO4 + 2H2O електролиза 2Cuo + O2 + 2H2SO4
Пример 2.6. Електролиза на разтвор на FeSO4
Тъй като желязото принадлежи към металите от група II, два конкурентни процеса ще протичат успоредно на катода (виж пример 2.3), а водата ще се окислява на анода (виж пример 2.4):
1-ви процес:
https://pandia.ru/text/80/299/images/image043_10.gif" width="41" height="12">2Fe2+ + 2Н2О el-z 2 Fe + O2 + 4H+ - йонно уравнение на процеса
2FeSO4 + 2Н2О el-z 2 Fe + O2 + 2Н2SO4– молекулно уравнение
2-ри процес:
K(+): 2H2O + 2ē → H2+ 2OH - *2
A(-): 2H2O - 4ē → O2+ 4H+
6H2O електролиза 2H2+ 4OH - + O2 + 4H+
6Н2О + 2FeSO4 електролиза 2Н2+ 2Fe(OH)2 + O2 + 2Н2SO4 - молекулярна
https://pandia.ru/text/80/299/images/image051_9.gif" width="21" height="50">И само ако процесите на катодна редукция на метални и водородни катиони от вода са в равни пропорции , можем да напишем общото крайно уравнение на реакцията:
(-) K: Fe2+ + 2ē → Fe0
2H2O + 2ē → H2+ 2HO - само 4 електрона
(+)A: 2H2O - 4ē → O2 + 4H+
Fe2+ + 2H2O + 2H2O → Fe + H2+ 2HO - + O2 + 4H+
2FeSO4 + 4Н2О el-z Fe + Н2+ Fe(OH)2 + O2 + 2Н2SO4
катоден анод
След изключване на тока и смесване на разтворите, крайното уравнение ще бъде както следва:
· Напишете уравнения за електролиза на разтвори на K2CO3, ZnSO4, AgNO3, NiI2, CoCl2.
· Решете проблем. За да се анализира съдържанието на примеси от NaCl в технически NaOH, 40 g от лекарството се разтварят във вода и се подлагат на електролиза до пълно окисление на хлорните йони. В този случай на анода се отделят 601 ml Cl2 при температура 200C и нормално налягане. Изчисли масова частПримеси на NaCl в NaOH.
3. Електролиза c разтворим с m анод
По-горе бяха разгледани примери за електролиза на водни разтвори на соли с инертен анод, т.е. такъв, който не участва химическо в анодния процес. Такива електроди са направени от неактивни благородни метали, като Pt, Ir или се използват въглеродни електроди. Ако се използват разтворими аноди, например Cu-анод, Zn-анод, тогава анодният процес се променя значително, тъй като самият анод се окислява. На анода на двата конкурентни протича процес с по-нисък потенциал: за окисление на мед E0 = - 0,34 V, за окисление на цинк E0 = - 0,76 V и за окисление на Cl анион , E0 = + 1,36 V.
Пример 3.1. Електролиза на воден разтвор на сол на CuCl2 с разтворим анод:
Катод (-): Cu-анод (+):
Сu2+ + 2ē → Cu0 Сu0 - 2ē → Cu2+
По този начин се получава един вид рафиниране на медния анод: той се разтваря, примесите остават в анодното пространство и върху катода се отлага чиста мед. Хлорният анион не се окислява, а се натрупва в анодното пространство.
Пример 3.2. Електролиза на воден разтвор на KCl сол с Cu анод:
Cu-анод (+): Сu0 - 2ē → Cu2+
В катода, в началния момент, водородът започва да се редуцира от вода, но появата на Cu2+ в разтвора прави две реакции на катодна редукция конкурентни:
K (-): 2H2O + 2ē → H2 + 2HO - E0 \u003d - 0,828 V
Cu2+ + 2ē → Cu0 E0 = + 0,34 V
В резултат на това протича предимно този, който се характеризира с по-висок потенциал, т.е. редукция на Сu2+ до Cu0.
Така в този случай ще настъпи разтваряне на Cu-анода: Сu0 - 2ē → Cu2+, а медните катиони, образувани на катода, ще се редуцират: Сu2+ + 2ē → Cu0. Солта KCl е необходима само за повишаване на електропроводимостта на разтвора и не участва пряко в редокс процесите.
Задание за самостоятелна работа.Да разгледаме електролизата на CuSO4 с Cu анод, Na2SO4 с Cu анод.
Електролиза на разтвор
и разтопени соли (2 часа)
Часове от избираемата дисциплина "Електрохимия"
Цели на първия урок:
Първи план на урока
1. Повтаряне на изучените методи за получаване на метали.
2. Обяснение на нов материал.
3. Решаване на задачи от учебника на Г. Е. Рудзитис, Ф. Г. Фелдман "Химия-9" (М .: Образование, 2002), стр. 120, № 1, 2.
4. Проверка на усвояването на знанията върху тестови задачи.
5. Доклад за приложението на електролизата.
Цели на първия урок:да научи как да пише схеми за електролиза на разтвори и стопени соли и да прилага получените знания за решаване на изчислителни задачи; продължи формирането на умения за работа с учебник, тестови материали; обсъждат приложението на електролизата в национална икономика.
ХОД НА ПЪРВИЯ УРОК
Повторение на изучени методи получаване на металина примера за получаване на мед от меден (II) оксид.
Записване на уравненията на съответните реакции:
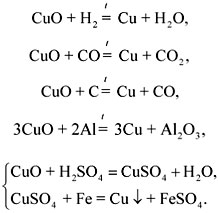
Друг начин за получаване на метали от разтвори и стопилки на техните соли е електрохимичен, или електролиза.
Електролизата е окислително-редукционен процес, който протича върху електродите, когато електрически ток преминава през стопилка или електролитен разтвор..
Електролиза на стопилка от натриев хлорид:
NaCl Na + + Cl – ;
катод (–) (Na +): Na + + д= Na 0,
анод (–) (Cl –): Cl – – д\u003d Cl 0, 2Cl 0 \u003d Cl 2;
2NaCl \u003d 2Na + Cl 2.
Електролиза на разтвор на натриев хлорид:
NaCl Na + + Cl – ,
H 2 O H + + OH-;
катод (–) (Na +; H +): H + + д= H 0 , 2H 0 = H 2
(2H 2 O + 2 д\u003d H 2 + 2OH -),
анод (+) (Cl - ; OH -): Cl - - д\u003d Cl 0, 2Cl 0 \u003d Cl 2;
2NaCl + 2H 2 O \u003d 2NaOH + Cl 2 + H 2.
Електролиза на разтвор на меден (II) нитрат:
Cu(NO 3) 2 Cu 2+ +
H 2 O H + + OH-;
катод (–) (Cu 2+; H +): Cu 2+ + 2 д= Cu 0 ,
анод (+) (OH -): OH - - д=OH0,
4H 0 \u003d O 2 + 2H 2 O;
2Cu(NO 3) 2 + 2H 2 O \u003d 2Cu + O 2 + 4HNO 3.
Тези три примера показват защо е по-изгодно да се извършва електролиза, отколкото да се извършват други методи за получаване на метали: получават се метали, хидроксиди, киселини, газове.
Написахме схемите за електролиза и сега ще се опитаме да напишем уравненията за електролиза веднага, без да се позоваваме на схемите, а само с помощта на скалата на йонната активност:
Примери за уравнения на електролиза:
2HgSO 4 + 2H 2 O \u003d 2Hg + O 2 + 2H 2 SO 4;
Na 2 SO 4 + 2H 2 O \u003d Na 2 SO 4 + 2H 2 + O 2;
2LiCl + 2H 2 O \u003d 2LiOH + H 2 + Cl 2.
Разрешаване на проблемот учебника на Г. Е. Рудзитис и Ф. Г. Фелдман (9 клас, стр. 120, № 1, 2).
Задача 1.По време на електролизата на разтвор на меден (II) хлорид масата на катода се е увеличила с 8 г. Какъв газ е бил отделен, каква е неговата маса?
Решение
CuCl 2 + H 2 O \u003d Cu + Cl 2 + H 2 O,
(Cu) \u003d 8/64 \u003d 0,125 mol,
(Cu) \u003d (Сl 2) \u003d 0,125 mol,
м(Cl 2) \u003d 0,125 71 \u003d 8,875 g.
Отговор. Газът е хлор с маса 8,875 g.
Задача 2.При електролизата на воден разтвор на сребърен нитрат се отделят 5,6 литра газ. Колко грама метал се отлага върху катода?
Решение
4AgNO 3 + 2H 2 O \u003d 4Ag + O 2 + 4HNO 3,
(O 2) \u003d 5,6 / 22,4 \u003d 0,25 mol,
(Ag) \u003d 4 (O 2) \u003d 4 25 \u003d 1 mol,
м(Ag) \u003d 1 107 \u003d 107 g.
Отговор. 107 г сребро.
Тестване
Опция 1
1. По време на електролизата на разтвор на калиев хидроксид на катода се отделя следното:
а) водород; б) кислород; в) калий.
2. По време на електролизата на разтвор на меден (II) сулфат в разтвор се образува следното:
а) меден(II) хидроксид;
б) сярна киселина;
3. По време на електролизата на разтвор на бариев хлорид на анода се отделя:
а) водород; б) хлор; в) кислород.
4. По време на електролиза на стопилка от алуминиев хлорид на катода се отделя следното:
а) алуминий; б) хлор;
в) електролизата е невъзможна.
5. Електролизата на разтвор на сребърен нитрат протича по следната схема:
а) AgNO 3 + H 2 O Ag + H 2 + HNO 3;
b) AgNO 3 + H 2 O Ag + O 2 + HNO 3;
в) AgNO 3 + H 2 O AgNO 3 + H 2 + O 2.
Вариант 2
1. По време на електролизата на разтвор на натриев хидроксид на анода се отделя следното:
а) натрий; б) кислород; в) водород.
2. По време на електролизата на разтвор на натриев сулфид в разтвор се образува следното:
а) сярноводородна киселина;
б) натриев хидроксид;
3. По време на електролизата на стопилка от живачен(II) хлорид на катода се отделя следното:
а) живак; б) хлор; в) електролизата е невъзможна.
4.
5. Електролизата на разтвор на живачен (II) нитрат протича по следната схема:
а) Hg (NO 3) 2 + H 2 O Hg + H 2 + HNO 3;
b) Hg (NO 3) 2 + H 2 O Hg + O 2 + HNO 3;
в) Hg (NO 3) 2 + H 2 O Hg (NO 3) 2 + H 2 + O 2.
Вариант 3
1. По време на електролизата на разтвор на меден (II) нитрат на катода се отделя:
а) мед; б) кислород; в) водород.
2. По време на електролизата на разтвор на литиев бромид в разтвор се образува следното:
б) бромоводородна киселина;
в) литиев хидроксид.
3. По време на електролизата на стопилка от сребърен хлорид на катода се отделя следното:
а) сребро; б) хлор; в) електролизата е невъзможна.
4. По време на електролизата на разтвор на алуминиев хлорид алуминият се освобождава в:
а) катод; б) анод; в) остава в разтвор.
5. Електролизата на разтвор на бариев бромид протича по следната схема:
а) BaBr 2 + H 2 O Br 2 + H 2 + Ba (OH) 2;
b) BaBr 2 + H 2 O Br 2 + Ba + H 2 O;
в) BaBr 2 + H 2 O Br 2 + O 2 + Ba (OH) 2.
Вариант 4
1. По време на електролизата на разтвор на бариев хидроксид на анода се отделя следното:
а) водород; б) кислород; в) барий.
2. По време на електролизата на разтвор на калиев йодид в разтвор се образува следното:
а) йодоводородна киселина;
б) вода; в) калиев хидроксид.
3. По време на електролиза на стопилка от оловен (II) хлорид на катода се отделя:
а) олово; б) хлор; в) електролизата е невъзможна.
4. По време на електролизата на разтвор на сребърен нитрат на катода се отделя следното:
а) сребро; б) водород; в) кислород.
5. Електролизата на разтвор на натриев сулфид протича по следната схема:
а) Na 2 S + H 2 O S + H 2 + NaOH;
b) Na 2 S + H 2 O H 2 + O 2 + Na 2 S;
в) Na 2 S + H 2 O H 2 + Na 2 S + NaOH.
Отговори
| опция | Въпрос 1 | Въпрос 2 | Въпрос 3 | Въпрос 4 | Въпрос 5 |
| 1 | А | b | b | А | b |
| 2 | b | b | А | А | b |
| 3 | А | V | А | V | А |
| 4 | b | V | А | А | А |
Използването на електролиза в националната икономика
1. За да предпазите металните продукти от корозия, върху тяхната повърхност се нанася тънък слой от друг метал: хром, сребро, злато, никел и др. Понякога, за да не се губят скъпи метали, се произвежда многослойно покритие. Например, външните части на автомобила първо се покриват с тънък слой мед, върху медта се нанася тънък слой никел и върху него се нанася слой хром.
При нанасяне на покрития върху метал чрез електролиза, те се получават равномерни по дебелина и издръжливи. По този начин можете да покриете продукти с всякаква форма. Този клон на приложната електрохимия се нарича галванопластика.
2. В допълнение към защитата от корозия, галваничните покрития придават красив декоративен вид на продуктите.
3. Друг клон на електрохимията, близък по принцип до галванопластиката, се нарича галванопластика. Това е процесът на получаване на точни копия на различни елементи. За да направите това, обектът се покрива с восък и се получава матрица. Всички вдлъбнатини на копирания обект върху матрицата ще бъдат издутини. Повърхността на восъчната матрица е покрита с тънък слой графит, което я прави електропроводима.
Полученият графитен електрод се потапя във вана с разтвор на меден сулфат. Анодът е меден. По време на електролизата медният анод се разтваря и медта се отлага върху графитния катод. Така се получава точно медно копие.
С помощта на електроформоването се изработват клишета за печат, грамофонни плочи, метализират се различни предмети. Галванопластиката е открита от руския учен Б. С. Якоби (1838 г.).
Изработването на матрици включва нанасяне на тънък слой сребро върху пластмасова плоча, за да стане електропроводима. След това върху плочата се нанася електролитно никелово покритие.
Какво трябва да се направи, за да се направи плоча в електролитна вана - анод или катод?
(Относно електронния катод.)
4. Електролизата се използва за получаване на много метали: алкални, алкалоземни, алуминий, лантаниди и др.
5. За да почистите някои метали от примеси, металът с примеси се свързва към анода. Металът се разтваря по време на процеса на електролиза и се утаява върху металния катод, докато примесът остава в разтвор.
6. Електролизата се използва широко за получаване на сложни вещества (алкали, кислородсъдържащи киселини), халогени.
Практическа работа(втори урок)
Цели на урока.Провеждане на електролиза на вода, показване на галванопластика на практика, консолидиране на знанията, получени в първия урок.
Оборудване.На студентските маси: празна батерия, два проводника с клеми, два графитни електрода, чаша, епруветки, триножник с два крака, 3% разтвор на натриев сулфат, спиртна лампа, кибрит, фенерче.
На бюрото на учителя: същото + разтвор на меден сулфат, месингов ключ, медна тръба (парче мед).
Инструктаж на студентите
1. Прикрепете проводниците с клеми към електродите.
2. Поставете електродите в чаша, така че да не се допират.
3. Изсипете електролитния разтвор (натриев сулфат) в чашата.
4. Налейте вода в епруветките и, като ги поставите с главата надолу в чаша с електролит, ги поставете върху графитните електроди един по един, като фиксирате горния ръб на епруветката в крака на статива.
5. След като устройството е монтирано, прикрепете краищата на проводниците към батерията.
6. Наблюдавайте еволюцията на газовите мехурчета: по-малко от тях се отделят на анода, отколкото на катода. След като почти цялата вода в една епруветка бъде изместена от освободения газ, а в другата - наполовина, изключете проводниците от батерията.
7. Запалете спиртната лампа, внимателно извадете епруветката, където водата е почти напълно изместена, и я поднесете към спиртната лампа - ще се чуе характерно пукане на газ.
8. Запалете факла. Отстранете втората епруветка, проверете с тлеещ газ.
Задачи за студенти
1. Скицирайте устройството.
2. Напишете уравнение за електролиза на вода и обяснете защо е необходимо да се извърши електролиза в разтвор на натриев сулфат.
3. Напишете уравнения на реакцията, които отразяват отделянето на газове върху електродите.
Учителски демонстрационен експеримент
(може да се изпълнява от най-добрите ученици в класа
с подходящо оборудване)
1. Свържете кабелните клеми към медната тръба и месинговия ключ.
2. Спуснете епруветката и ключа в чаша с разтвор на меден (II) сулфат.
3. Свържете вторите краища на проводниците към батерията: "минус" на батерията към медната тръба, "плюс" към ключа!
4. Наблюдавайте отделянето на мед върху повърхността на ключа.
5. След като извършите експеримента, първо изключете клемите от батерията, след което извадете ключа от разтвора.
6. Разглобете веригата за електролиза с разтворим електрод:
CuSO 4 \u003d Cu 2+ +
анод (+): Сu 0 - 2 д\u003d Cu 2+,
катод (–): Cu 2+ + 2 д= Сu 0 .
Общото уравнение за електролиза с разтворим анод не може да бъде написано.
Електролизата се извършва в разтвор на меден (II) сулфат, тъй като:
а) необходим е електролитен разтвор, за да протича електрически ток, т.к. водата е слаб електролит;
б) няма да се отделят странични продукти от реакциите, а само мед на катода.
7. За да консолидирате миналото, напишете схема за електролиза на цинков хлорид с въглеродни електроди:
ZnCl 2 \u003d Zn 2+ + 2Cl -,
катод (–): Zn 2+ + 2 д= Zn 0,
2H2O+2 д\u003d H 2 + 2OH -,
анод (+): 2Cl – – 2 д=Cl2.
Общото уравнение на реакцията в този случай не може да бъде написано, т.к не е известно каква част от общото количество електроенергия отива за редукция на вода и каква част - за редукция на цинкови йони.
 |
Схема на демонстрационния експеримент |
Домашна работа
1. Напишете уравнение за електролиза на разтвор, съдържащ смес от меден (II) нитрат и сребърен нитрат с инертни електроди.
2. Напишете уравнението за електролизата на разтвор на натриев хидроксид.
3. За да почистите медна монета, тя трябва да бъде окачена на медна жица, свързана към отрицателния полюс на батерията, и спусната в 2,5% разтвор на NaOH, където трябва да бъде потопен и графитният електрод, свързан към положителния полюс на батерията . Обяснете как една монета става чиста. ( Отговор. Водородните йони се редуцират на катода:
2H + + 2 д\u003d H 2.
Водородът реагира с меден оксид на повърхността на монетата:
CuO + H 2 \u003d Cu + H 2 O.
Този метод е по-добър от почистването с прах, т.к. монетата не се изтрива.)
ЕЛЕКТРОЛИЗА
Един от начините за получаване на метали е електролизата. Активните метали се срещат в природата само под формата на химични съединения. Как да се изолира от тези съединения в свободно състояние?
Разтворите и стопилките на електролитите провеждат електрически ток. Въпреки това, когато ток преминава през електролитен разтвор, могат да възникнат химични реакции. Помислете какво ще се случи, ако две метални пластини се поставят в електролитен разтвор или стопилка, всяка от които е свързана към един от полюсите на източника на ток. Тези пластини се наричат електроди. Електрическият ток е движещ се поток от електрони. В резултат на факта, че електроните във веригата се движат от един електрод към друг, на един от електродите се появява излишък от електрони. Електроните имат отрицателен заряд, така че този електрод става отрицателно зареден. Нарича се катод. На другия електрод се създава липса на електрони и той е положително зареден. Този електрод се нарича анод. Електролитът в разтвор или стопилка се разпада на положително заредени йони - катиони и отрицателно заредени йони - аниони. Катионите се привличат към отрицателно зареден електрод - катод. Анионите се привличат към положително зареден електрод - анод. На повърхността на електродите може да възникне взаимодействие между йони и електрони.
Електролизата се отнася до процесите, които възникват, когато електрически ток преминава през разтвори или стопилки на електролити.
Процесите, протичащи по време на електролиза на разтвори и стопилки на електролити, са доста различни. Нека разгледаме и двата случая в детайли.
Електролиза на стопилка
Като пример, разгледайте електролизата на стопилка от натриев хлорид. В стопилката натриевият хлорид се разпада на йони Na+
и Cl - : NaCl = Na + + Cl -
Натриевите катиони се придвижват към повърхността на отрицателно зареден електрод - катод. На повърхността на катода има излишък от електрони. Следователно има прехвърляне на електрони от повърхността на електрода към натриеви йони. В същото време йони Na+ се превръщат в натриеви атоми, т.е. катионите се редуцират Na+ . Уравнение на процеса:
Na + + e - = Na
Хлоридни йони Cl - се придвижват към повърхността на положително зареден електрод - анода. На повърхността на анода се създава липса на електрони и електроните се прехвърлят от аниони Cl- към повърхността на електрода. В същото време отрицателно заредени йони Cl- се превръщат в хлорни атоми, които веднага се комбинират, за да образуват хлорни молекули C l2:
2C l - -2e - \u003d Cl 2
Хлоридните йони губят електрони, тоест се окисляват.
Нека напишем заедно уравненията на процесите, протичащи на катода и анода
Na + + e - = Na
2 C l - -2 e - \u003d Cl 2
Един електрон участва в процеса на редукция на натриеви катиони, а 2 електрона участват в процеса на окисление на хлорни йони. Трябва обаче да се спазва законът за запазване на електрическия заряд, тоест общият заряд на всички частици в разтвора трябва да бъде постоянен.Следователно броят на електроните, участващи в редукция на натриевите катиони, трябва да бъде равен на броя на електроните участващи в окисляването на хлоридните йони. Следователно умножаваме първото уравнение по 2:
Na + + e - \u003d Na 2
2C l - -2e - \u003d Cl 2 1
Събираме двете уравнения заедно и получаваме общото уравнение на реакцията.
2 Na + + 2C l - \u003d 2 Na + Cl 2 (уравнение на йонна реакция), или
2 NaCl \u003d 2 Na + Cl 2 (уравнение на молекулярна реакция)
И така, в разглеждания пример виждаме, че електролизата е редокс реакция. На катода, редукция на положително заредени йони - катиони, на анода - окисление на отрицателно заредени йони - аниони. За да запомните кой процес къде се случва, можете да използвате "правилото T":
катод - катион - редукция.
Пример 2Електролиза на стопилка от натриев хидроксид.
Натриевият хидроксид в разтвор се дисоциира на катиони и хидроксидни йони.
катод (-)<-- Na + + OH - à Анод (+)
На повърхността на катода натриевите катиони се редуцират и се образуват натриеви атоми:
катод (-) Na + +e à Na
Хидроксидните йони се окисляват на повърхността на анода, докато се освобождава кислород и се образуват водни молекули:
катод (-) Na + + e à Na
анод (+)4 OH - - 4 e à 2 H 2 O + O 2
Броят на електроните, участващи в реакцията на редукция на натриевите катиони и в реакцията на окисление на хидроксидните йони, трябва да бъде еднакъв. Нека умножим първото уравнение по 4:
катод (-) Na + + e à Na 4
анод (+)4 OH - – 4 e à 2 H 2 O + O 2 1
Събирайки двете уравнения заедно, получаваме уравнението за реакцията на електролиза:
4 NaOH до 4 Na + 2 H 2 O + O 2
Пример 3Помислете за електролизата на стопилката Al2O3
Използвайки тази реакция, алуминият се получава от боксит, естествено съединение, което съдържа много алуминиев оксид. Точката на топене на алуминиевия оксид е много висока (повече от 2000º C), така че към него се добавят специални добавки, понижаващи точката на топене до 800-900º C. В стопилката алуминиевият оксид се разпада на йони Al 3+ и O 2-. з катионите се редуцират на катодаАл 3+ , превръщайки се в алуминиеви атоми:
Al +3 e a Al
Анионите се окисляват на анодаО 2- превръщайки се в кислородни атоми. Кислородните атоми веднага се комбинират в O 2 молекули:
2 O 2- – 4 e à O 2
Броят на електроните, участващи в редукцията на алуминиевите катиони и окисляването на кислородните йони, трябва да бъде равен, така че умножаваме първото уравнение по 4, а второто по 3:
Al 3+ +3 e à Al 0 4
2 O 2- – 4 e à O 2 3
Нека съберем двете уравнения и ще получим
4 Al 3+ + 6 O 2- a 4 Al 0 +3 O 2 0 (уравнение на йонна реакция)
2 Al 2 O 3 до 4 Al + 3 O 2
Електролиза на разтвор
В случай на преминаване на електрически ток през воден разтвор на електролит, въпросът се усложнява от наличието на водни молекули в разтвора, които също могат да взаимодействат с електрони. Спомнете си, че във водната молекула водородните и кислородните атоми са свързани чрез полярна ковалентна връзка. Електроотрицателността на кислорода е по-голяма от електроотрицателността на водорода, така че споделените електронни двойки са изместени към кислородния атом. На кислородния атом възниква частичен отрицателен заряд, който се обозначава с δ-, а на водородните атоми има частичен положителен заряд, който се обозначава с δ+.
δ+
H-O δ-
│
H δ+
Поради това изместване на зарядите водната молекула има положителни и отрицателни "полюси". Следователно водните молекули могат да бъдат привлечени от положително зареден полюс към отрицателно зареден електрод - катод, и чрез отрицателен полюс - към положително зареден електрод - анод. На катода водните молекули могат да се редуцират и се отделя водород:
Окисляването на водните молекули може да настъпи на анода с освобождаване на кислород:
2 H 2 O - 4e - \u003d 4H + + O 2
Следователно или електролитни катиони, или водни молекули могат да бъдат редуцирани на катода. Тези два процеса изглежда се конкурират един с друг. Какъв процес всъщност протича на катода зависи от естеството на метала. Дали металните катиони или водните молекули ще бъдат редуцирани на катода зависи от позицията на метала в серия от метални напрежения .
Li K Na Ca Mg Al ¦¦ Zn Fe Ni Sn Pb (H 2) ¦¦ Cu Hg Ag Au
Ако металът е в серията напрежения вдясно от водорода, металните катиони се редуцират на катода и се освобождава свободен метал. Ако металът е в серията напрежения вляво от алуминия, водните молекули се редуцират на катода и се освобождава водород. И накрая, в случай на метални катиони от цинк до олово може да настъпи или отделяне на метал, или отделяне на водород, а понякога и водород, и метал се отделят едновременно. Като цяло това е доста сложен случай, много зависи от условията на реакцията: концентрацията на разтвора, силата на тока и други.
Един от двата процеса може да се случи и на анода - или окисление на електролитни аниони, или окисление на водни молекули. Кой процес действително се осъществява зависи от природата на аниона. По време на електролизата на соли на аноксикиселините или на самите киселини анионите се окисляват на анода. Единственото изключение е флуоридният йонФ- . При кислородсъдържащите киселини водните молекули се окисляват на анода и се отделя кислород.
Пример 1Нека разгледаме електролизата на воден разтвор на натриев хлорид.
Във воден разтвор на натриев хлорид ще има натриеви катиони Na + , хлорни аниони Cl - и водни молекули.
2 NaCl a 2 Na + + 2 Cl -
2Н 2 О а 2 H + + 2 OH -
катод (-) 2 Na + ; 2 Н+; 2Н + + 2е а Н 0 2
анод (+) 2 Cl - ; 2OH-; 2 Cl - – 2e a 2 Cl 0
2NaCl + 2H 2 O до H 2 + Cl 2 + 2NaOH
химически дейност аниони едва ли намалява.
Пример 2Ами ако солта съдържа SO 4 2- ? Помислете за електролиза на разтвор на никелов сулфат ( II ). никелов сулфат ( II ) дисоциира на йони Ni 2+ и SO 4 2-:
NiSO 4 à Ni 2+ + SO 4 2-
H 2 O à H + + OH -
Никеловите катиони са между металните йони Al 3+ и Pb 2+ , заемайки средно положение в серията на напрежението, процесът на възстановяване на катода протича и по двете схеми:
2 H 2 O + 2e - \u003d H 2 + 2OH -
Анионите на кислородсъдържащите киселини не се окисляват на анода ( серия от анионна активност ), водните молекули се окисляват:
анод e à O 2 + 4H +
Нека напишем заедно уравненията на процесите, протичащи на катода и анода:
катод (-) Ni 2+ ; Н+; Ni 2+ + 2е а Ni 0
2 H 2 O + 2e - \u003d H 2 + 2OH -
анод (+) SO42-; OH -; 2H 2 O - 4 e à O 2 + 4H +
В процесите на редукция участват 4 електрона, а в процеса на окисляване също участват 4 електрона. Събирайки тези уравнения заедно, получаваме общото уравнение на реакцията:
Ni 2+ +2 H 2 O + 2 H 2 O à Ni 0 + H 2 + 2OH - + O 2 + 4 H +
От дясната страна на уравнението има едновременно Н + йони ио- , които се комбинират, за да образуват водни молекули:
H + + OH - à H 2 O
Следователно, от дясната страна на уравнението, вместо 4 H + йона и 2 йонао- пишем 2 водни молекули и 2 Н + йона:
Ni 2+ +2 H 2 O + 2 H 2 O à Ni 0 + H 2 +2 H 2 O + O 2 + 2 H +
Нека намалим две водни молекули от двете страни на уравнението:
Ni 2+ +2 H 2 O à Ni 0 + H 2 + O 2 + 2 H +
Това е кратко йонно уравнение. За да получите пълното йонно уравнение, трябва да добавите към двете части сулфатния йон SO 4 2- , образуван по време на дисоциацията на никелов сулфат ( II ) и не участва в реакцията:
Ni 2+ + SO 4 2- + 2H 2 O à Ni 0 + H 2 + O 2 + 2H + + SO 4 2-
Така по време на електролизата на разтвор на никелов сулфат ( II ) на катода се отделят водород и никел, а на анода - кислород.
NiSO 4 + 2H 2 O à Ni + H 2 + H 2 SO 4 + O 2
Пример 3 Напишете уравненията на процесите, протичащи по време на електролизата на воден разтвор на натриев сулфат с инертен анод.
Стандартен електроден потенциал на системата Na + + e = Na 0 е много по-отрицателен от потенциала на водния електрод в неутрална водна среда (-0,41 V). Следователно на катода ще настъпи електрохимична редукция на водата, придружена от отделяне на водород
2Н 2 О а 2 H + + 2 OH -
и Na йони + идващи към катода ще се натрупват в съседната част на разтвора (катодно пространство).
На анода ще настъпи електрохимично окисление на водата, което ще доведе до освобождаване на кислород.
2 H 2 O - 4e à O 2 + 4 H +
тъй като съответстващи на тази система стандартен електроден потенциал (1,23 V) е значително по-нисък от стандартния електроден потенциал (2,01 V), който характеризира системата
2 SO 4 2- + 2 e \u003d S 2 O 8 2-.
Йони SO 4 2- движещи се към анода по време на електролиза ще се натрупат в анодното пространство.
Умножавайки уравнението на катодния процес по две и го добавяйки с уравнението на анодния процес, получаваме общото уравнение на процеса на електролиза:
6 H 2 O \u003d 2 H 2 + 4 OH - + O 2 + 4 H +
Като се има предвид, че йоните се натрупват едновременно в катодното пространство и йоните в анодното пространство, общото уравнение на процеса може да бъде написано в следната форма:
6H 2 O + 2Na 2 SO 4 \u003d 2H 2 + 4Na + + 4OH - + O 2 + 4H + + 2SO 4 2-
Така едновременно с отделянето на водород и кислород се образуват натриев хидроксид (в катодното пространство) и сярна киселина (в анодното пространство).
Пример 4Електролиза на разтвор на меден сулфат ( II) CuSO4.
катод (-)<-- Cu 2+ + SO 4 2- à анод (+)
катод (-) Cu 2+ + 2e à Cu 0 2
анод (+) 2H 2 O - 4 e à O 2 + 4H + 1
В разтвора остават Н + йони и SO 4 2- , тъй като се натрупва сярна киселина.
2CuSO 4 + 2H 2 O до 2Cu + 2H 2 SO 4 + O 2
Пример 5 Електролиза на разтвор на меден хлорид ( II) CuCl2.
катод (-)<-- Cu 2+ + 2Cl - à анод (+)
катод (-) Cu 2+ + 2e à Cu 0
анод (+) 2Cl - – 2e à Cl 0 2
И двете уравнения включват два електрона.
Cu 2+ + 2e à Cu 0 1
2Cl - --– 2e à Cl 2 1
Cu 2+ + 2 Cl - à Cu 0 + Cl 2 (йонно уравнение)
CuCl 2 до Cu + Cl 2 (молекулно уравнение)
Пример 6 Електролиза на разтвор на сребърен нитрат AgNO3.
катод (-)<-- Ag + + NO 3 - à Анод (+)
катод (-) Ag + + e à Ag 0
анод (+) 2H 2 O - 4 e à O 2 + 4H +
Ag + + e à Ag 0 4
2H 2 O - 4 e à O 2 + 4H + 1
4 Ag + + 2 H 2 O à 4 Ag 0 + 4 H + + О 2 (йонно уравнение)
4 Ag + + 2 з 2 Оà 4 Ag 0 + 4 з + + О 2 + 4 НЕ 3 - (пълно йонно уравнение)
4 AgNO 3 + 2 з 2 Оà 4 Ag 0 + 4 HNO 3 + О 2 (молекулно уравнение)
Пример 7 Електролиза на разтвор на солна киселинаНС1.
катод (-)<-- з + + кл - à анод (+)
катод (-) 2з + + 2 дà з 2
анод (+) 2кл - – 2 дà кл 2
2 з + + 2 кл - à з 2 + кл 2 (йонно уравнение)
2 НС1à з 2 + кл 2 (молекулно уравнение)
Пример 8 Електролиза на разтвор на сярна киселиназ 2 ТАКА 4 .
Катод (-) <-- 2H + + SO 4 2- à анод (+)
катод (-)2Н+ + 2еà H2
анод(+) 2H 2 O - 4дà О2+4Н+
2Н+ + 2еà H 2 2
2H2O-4дà О2 + 4Н+1
4H+ + 2H2Oà 2H 2 + 4H + + O 2
2H2Oà 2H2+O2
Пример 9. Електролиза на разтвор на калиев хидроксидKOH.
катод (-)<-- К + + о - à анод (+)
Калиевите катиони няма да бъдат редуцирани на катода, тъй като калият е в серията напрежения на металите вляво от алуминия, вместо това водните молекули ще бъдат редуцирани:
2H2O + 2eà Н 2 + 2ОН - 4ОН - -4еà 2H 2 O + O 2
катод(-)2H2O+2eà Н 2 + 2ОН - 2
анод(+) 4OH - - 4eà 2H 2 O + O 2 1
4H 2 O + 4OH -à 2H 2 + 4OH - + 2H 2 O + O 2
2 з 2 Оà 2 з 2 + О 2
Пример 10 Електролиза на разтвор на калиев нитратKNO 3 .
Катод (-) <-- K + + NO 3 - à анод (+)
2H2O + 2eà Н 2 + 2ОН - 2Н 2 О - 4дà О2+4Н+
катод(-)2H2O+2eà Н2 + 2ОН-2
анод(+) 2H 2 O - 4дà О2 + 4Н+1
4H2O + 2H2Oà 2Н2+4ОН-+4Н++ O2
2H2Oà 2H2+O2
При преминаване на електрически ток през разтвори на кислородсъдържащи киселини, алкали и соли на кислородсъдържащи киселини с метали, които са в серията на напрежението на металите, вляво от алуминия, практически се получава електролиза на водата. В този случай на катода се отделя водород, а на анода - кислород.
Изводи. При определяне на продуктите от електролизата на водни разтвори на електролити в най-простите случаи може да се ръководи от следните съображения:
1. Метални йони с малка алгебрична стойност на стандартния потенциал - отЛи + предиАл 3+ включително - имат много слаба тенденция да прикрепят отново електрони, отстъпвайки в това отношение на йониз + (см. Серия от активност на катиони). При електролизата на водни разтвори на съединения, съдържащи тези катиони, функцията на окислител на катода се изпълнява от йониз + , докато възстановявате по схемата:
2 з 2 О+ 2 дà з 2 + 2OH -
2. Метални катиони с положителни стойности на стандартните потенциали (Cu 2+ , Ag + , hg 2+ и т.н.) имат по-голяма склонност да прикрепват електрони, отколкото йони. По време на електролизата на водни разтвори на техните соли, тези катиони излъчват функцията на окислител на катода, докато се редуцират до метал съгласно схемата, например:
Cu 2+ +2 дà Cu 0
3. По време на електролизата на водни разтвори на метални солиZn, Fe, CD, Niи други, заемащи средно положение между изброените групи в серията на напрежението, процесът на редукция на катода протича и по двете схеми. Масата на освободения метал в тези случаи не съответства на количеството протичащ електрически ток, част от който се изразходва за образуването на водород.
4. Във водни разтвори на електролити, едноатомни аниони (кл - , бр - , Дж - ), кислородсъдържащи аниони (НЕ 3 - , ТАКА 4 2- , PO 4 3- и други), както и хидроксилните йони на водата. От тях халидните йони имат по-силни редуциращи свойства, с изключение наЕ. йониозаемат междинно положение между тях и многоатомните аниони. Следователно, по време на електролизата на водни разтвориНС1, HBr, HJили техните соли върху анода, халидните йони се окисляват по схемата:
2 х - -2 дà х 2 0
При електролизата на водни разтвори на сулфати, нитрати, фосфати и др. функцията на редуциращия агент се изпълнява от йони, докато се окислява по схемата:
4 ХОХ – 4 дà 2 з 2 О + О 2 + 4 з +
.
Задачи.
З А дача 1. По време на електролизата на разтвор на меден сулфат на катода се отделят 48 g мед. Намерете обема на газа, отделен на анода, и масата на сярната киселина, образувана в разтвора.
Медният сулфат в разтвора не дисоциира нито един от йонитеC 2+ иС0 4 2 ".
CuS0 4 \u003d Cu 2+ + S0 4 2 "
Нека напишем уравненията на процесите, протичащи на катода и анода. Cu катионите се редуцират на катода, електролизата на водата се извършва на анода:
Cu 2+ + 2e- \u003d Cu12
2H 2 0-4e- = 4H + + 0 2 |1
Общо уравнение на електролизата:
2Cu2+ + 2H2O = 2Cu + 4H+ + O2 (кратко йонно уравнение)
Добавете към двете страни на уравнението по 2 сулфатни йона, които се образуват по време на дисоциацията на меден сулфат, получаваме пълното йонно уравнение:
2Cu2+ + 2S042" + 2H20 = 2Cu + 4H+ + 2SO4 2" + O2
2CuSO4 + 2H2O = 2Cu + 2H2SO4 + O2
Газът, отделен на анода, е кислород. В разтвора се образува сярна киселина.
Моларната маса на медта е 64 g / mol, изчисляваме количеството медно вещество:
Според уравнението на реакцията, когато 2 mol мед се отделят от анода, се освобождава 1 mol кислород. 0,75 mol мед се отделя на катода, нека x mol кислород се отделя на анода. Да направим пропорция:
2/1=0,75/x, x=0,75*1/2=0,375mol
На анода се отделя 0,375 mol кислород,
v(O2) = 0,375 mol.
Изчислете обема на отделения кислород:
V(O2) \u003d v (O2) "VM \u003d 0,375 mol" 22,4 l / mol \u003d 8,4 l
Според уравнението на реакцията, когато на катода се отделят 2 mol мед, в разтвора се образуват 2 mol сярна киселина, което означава, че ако на катода се отделят 0,75 mol мед, тогава се образува 0,75 mol сярна киселина в разтвора, v (H2SO4) = 0,75 mol . Изчислете моларната маса на сярната киселина:
M(H2SO4) = 2-1+32+16-4 = 98 g/mol.
Изчислете масата на сярната киселина:
m (H2S04) \u003d v (H2S04> M (H2S04) \u003d = 0,75 mol = 98 g / mol = 73,5 g.
Отговор:На анода са отделени 8,4 литра кислород; В разтвора се образуват 73,5 g сярна киселина
Задача 2. Намерете обема на газовете, отделени на катода и анода по време на електролизата на воден разтвор, съдържащ 111,75 g калиев хлорид. Какво вещество се образува в разтвора? Намерете масата му.
Калиевият хлорид в разтвор се дисоциира на K+ и Cl йони:
2KS1 \u003d K + + Cl
Калиевите йони не се редуцират на катода; вместо това се редуцират водните молекули. Хлоридните йони се окисляват на анода и се отделя хлор:
2H2O + 2e "= H2 + 20H-|1
2SG-2e "= C12|1
Общо уравнение на електролизата:
2CHl + 2H2O \u003d H2 + 2OH "+ C12 (кратко йонно уравнение) Разтворът също съдържа K + йони, образувани по време на дисоциацията на калиев хлорид и не участващи в реакцията:
2K+ + 2Cl + 2H20 = H2 + 2K+ + 2OH" + C12
Нека пренапишем уравнението в молекулярна форма:
2KS1 + 2H2O = H2 + C12 + 2KOH
Водородът се отделя на катода, хлорът се отделя на анода и се образува калиев хидроксид в разтвор.
Разтворът съдържа 111,75 g калиев хлорид.
Изчислете моларната маса на калиев хлорид:
M(KC1) = 39+35,5 = 74,5 g/mol
Изчислете количеството вещество калиев хлорид:

Според уравнението на реакцията при електролиза на 2 mol калиев хлорид се отделя 1 mol хлор. Нека електролизата на 1,5 mol калиев хлорид освободи x mol хлор. Да направим пропорция:
2/1=1,5/x, x=1,5 /2=0,75 mol
Ще се отделят 0,75 mol хлор, v (C! 2) \u003d 0,75 mol. Според уравнението на реакцията, когато 1 mol хлор се отделя на анода, 1 mol водород се освобождава на катода. Следователно, ако на анода се отделят 0,75 mol хлор, тогава на катода се отделят 0,75 mol водород, v(H2) = 0,75 mol.
Нека изчислим обема на хлора, отделен на анода:
V (C12) \u003d v (Cl2) -VM \u003d 0,75 mol = 22,4 l / mol = 16,8 l.
Обемът на водорода е равен на обема на хлора:
Y (H2) \u003d Y (C12) \u003d 16,8 л.
Според уравнението на реакцията при електролизата на 2 mol калиев хлорид се образуват 2 mol калиев хидроксид, което означава, че при електролизата на 0,75 mol калиев хлорид се образуват 0,75 mol калиев хидроксид. Изчислете моларната маса на калиев хидроксид:
M (KOH) \u003d 39 + 16 + 1 - 56 g / mol.
Изчислете масата на калиев хидроксид:
m(KOH) \u003d v (KOH> M (KOH) \u003d 0,75 mol-56 g / mol \u003d 42 g.
Отговор:На катода са отделени 16,8 литра водород, на анода са отделени 16,8 литра хлор и в разтвора се образуват 42 g калиев хидроксид.
Задача 3. При електролизата на разтвор от 19 g двувалентен метален хлорид на анода се отделят 8,96 литра хлор. Определете кой метален хлорид е бил подложен на електролиза. Изчислете обема на водорода, отделен на катода.
Означаваме неизвестния метал M, формулата на неговия хлорид е MC12. На анода хлоридните йони се окисляват и се отделя хлор. Условието казва, че на катода се отделя водород, следователно водните молекули се редуцират:
2H20 + 2e- = H2 + 2OH|1
2Cl -2e "= C12! 1
Общо уравнение на електролизата:
2Cl + 2H2O \u003d H2 + 2OH "+ C12 (кратко йонно уравнение)
Разтворът също така съдържа M2+ йони, които не се променят по време на реакцията. Пишем пълното уравнение на йонната реакция:
2SG + M2+ + 2H2O = H2 + M2+ + 2OH- + C12
Нека пренапишем уравнението на реакцията в молекулярна форма:
MS12 + 2H2O - H2 + M(OH)2 + C12
Намерете количеството хлор, отделено на анода:
![]()
Според уравнението на реакцията по време на електролизата на 1 mol хлорид на неизвестен метал се отделя 1 mol хлор. Ако се отделят 0,4 mol хлор, тогава 0,4 mol метален хлорид се подлага на електролиза. Изчислете моларната маса на металния хлорид:
Моларната маса на хлорида на неизвестен метал е 95 g/mol. Има 35,5"2 = 71 g/mol на два хлорни атома. Следователно моларната маса на метала е 95-71 = 24 g/mol. Магнезият съответства на тази моларна маса.
Според уравнението на реакцията, за 1 мол хлор, отделен на анода, има 1 мол водород, отделен на катода. В нашия случай на анода се отделя 0,4 mol хлор, което означава, че на катода се отделя 0,4 mol водород. Изчислете обема на водорода:
V (H2) \u003d v (H2> VM \u003d 0,4 mol = 22,4 l / mol \u003d 8,96 l.
Отговор:подложен на електролиза разтвор на магнезиев хлорид; На катода са отделени 8,96 литра водород.
*Задача 4. При електролизата на 200 g разтвор на калиев сулфат с концентрация 15% на анода се отделят 14,56 литра кислород. Изчислете концентрацията на разтвора в края на електролизата.
В разтвор на калиев сулфат водните молекули реагират както на катода, така и на анода:
2H20 + 2e "= H2 + 20H-|2
2H2O - 4e "= 4H+ + O2! 1
Нека съберем двете уравнения заедно:
6H2O \u003d 2H2 + 4OH "+ 4H + + O2, или
6H2O \u003d 2H2 + 4H2O + O2, или
2H2O = 2H2 + 02
Всъщност по време на електролизата на разтвор на калиев сулфат се получава електролиза на вода.
Концентрацията на разтвореното вещество в разтвор се определя по формулата:
C=m(разтвор) 100% / m(разтвор)
За да се намери концентрацията на разтвора на калиев сулфат в края на електролизата, е необходимо да се знае масата на калиевия сулфат и масата на разтвора. Масата на калиев сулфат не се променя по време на реакцията. Изчислете масата на калиевия сулфат в първоначалния разтвор. Нека обозначим концентрацията на първоначалния разтвор като С
m(K2S04) = C2 (K2S04) m(разтвор) = 0,15 200 g = 30 g.
Масата на разтвора се променя по време на електролиза, тъй като част от водата се превръща във водород и кислород. Изчислете количеството освободен кислород:
(О 2) \u003d V (O2) / Vm \u003d 14,56 l / 22,4 l / mol \u003d 0,65 mol
Според уравнението на реакцията 1 мол кислород се образува от 2 мола вода. Нека при разлагането на x mol вода се отделят 0,65 mol кислород. Да направим пропорция:
![]()
1,3 mol вода се разлага, v(H2O) = 1,3 mol.
Изчислете моларната маса на водата:
M(H2O) \u003d 1-2 + 16 \u003d 18 g / mol.
Изчислете масата на разложената вода:
m(H2O) \u003d v (H2O> M (H2O) \u003d 1,3 mol * 18 g / mol \u003d 23,4 g.
Масата на разтвора на калиев сулфат намалява с 23,4 g и става равна на 200-23,4 = 176,6 g. Сега нека изчислим концентрацията на разтвора на калиев сулфат в края на електролизата:
С2 (K2 SO4)=m(K2 SO4) 100% / m(разтвор)=30g 100% / 176.6g=17%
Отговор:концентрацията на разтвора в края на електролизата е 17%.
* 3 задача 5. 188,3 g смес от натриев и калиев хлориди се разтварят във вода и през получения разтвор се пропуска електрически ток. По време на електролиза на катода са отделени 33,6 литра водород. Изчислете състава на сместа в тегловни проценти.
След разтваряне на смес от калиеви и натриеви хлориди във вода, разтворът съдържа K+, Na+ и Cl- йони. Нито калиевите йони, нито натриевите йони се редуцират на катода, водните молекули се редуцират. Хлоридните йони се окисляват на анода и се отделя хлор:
Нека пренапишем уравненията в молекулярна форма:
2KS1 + 2H20 = H2 + C12 + 2KOH
2NaCl + 2H2O = H2 + C12 + 2NaOH
Нека обозначим количеството вещество калиев хлорид, съдържащо се в сместа, x mol, и количеството вещество натриев хлорид, y mol. Според уравнението на реакцията при електролизата на 2 mol натриев или калиев хлорид се отделя 1 mol водород. Следователно по време на електролиза x mol калиев хлорид се образува x / 2 или 0,5x mol водород, а по време на електролиза y mol натриев хлорид е 0,5y mol водород. Да намерим количеството водородни вещества, отделени по време на електролизата на сместа:
![]()
Нека съставим уравнението: 0,5x + 0,5y \u003d 1,5
Изчислете моларните маси на калиеви и натриеви хлориди:
M(KC1) = 39+35,5 = 74,5 g/mol
M (NaCl) \u003d 23 + 35,5 \u003d 58,5 g / mol
Масата x mol калиев хлорид е:
m (KCl) \u003d v (KCl) -M (KCl) \u003d x mol-74,5 g / mol \u003d 74,5 x g.
Масата на мол натриев хлорид е:
m (KCl) \u003d v (KCl) -M (KCl) \u003d y mol-74,5 g / mol \u003d 58,5 u g.
Масата на сместа е 188,3 g, правим второто уравнение:
74,5x + 58,5y = 188,3
И така, решаваме система от две уравнения с две неизвестни:
0,5(x + y)= 1,5
74.5x + 58.5y = 188.3g
От първото уравнение изразяваме x:
x + y \u003d 1,5 / 0,5 \u003d 3,
x = 3-y
Замествайки тази стойност на x във второто уравнение, получаваме:
74,5-(3-y) + 58,5y = 188,3
223,5-74,5y + 58,5y = 188,3
-16y = -35,2
y \u003d 2,2 100% / 188,3g \u003d 31,65%
Изчислете масовата част на натриевия хлорид:
w(NaCl) = 100% - w(KCl) = 68,35%
Отговор:сместа съдържа 31,65% калиев хлорид и 68,35% натриев хлорид.
Когато се разглежда електролизата на разтвори, не трябва да се изпуска от поглед факта, че в допълнение към електролитните йони във всеки воден разтвор има и йони, които все още са продукти на дисоциацията на водата - Н + и ОН -. поле, водородните йони се придвижват към катода, а хидроксилните към анода. По този начин, както електролитните катиони, така и водородните катиони могат да бъдат разредени на катода. По същия начин, в анода, както електролитните аниони, така и хидроксилните йони могат да бъдат разредени. В допълнение, водните молекули също могат да претърпят електрохимично окисление или редукция.
Кои електрохимични процеси ще протичат на електродите по време на електролиза, ще зависи преди всичко от съотношението на електродните потенциали на съответните електрохимични системи. Това означава, че окислените форми на електрохимичните системи ще бъдат редуцирани на катода. От няколкото възможни процеса ще протече този с минимален разход на енергия. Това означава, че окислените форми на електрохимичните системи с най-висок електроден потенциал ще бъдат редуцирани на катода, докато редуцираните форми на системите с най-нисък електроден потенциал ще бъдат окислени на анода. Електродният материал има инхибиторен ефект върху протичането на някои електрохимични процеси; такива случаи са разгледани по-долу.
Като се имат предвид катодните процеси, протичащи по време на електролизата на водни разтвори, е необходимо да се вземе предвид стойността на потенциала на процеса на редукция на водородни йони. Този потенциал зависи от концентрацията на водородните йони и в случай на неутрални разтвори (рН=7) има стойност
φ \u003d -0,059 * 7 \u003d -0,41 V. От това става ясно, че ако електролитът е образуван от метал, чийто електроден потенциал е много по-положителен от -0,41 V, тогава металът ще бъде освободен от неутралния разтвор при катод. Такива метали са в поредица от напрежения близо до водорода (започвайки приблизително от калай) и след него. Напротив, в случай на електролити, чийто метал има потенциал много по-отрицателен от –0,41 V, металът няма да се редуцира, но ще се отдели водород. Такива метали включват метали в началото на поредица от напрежения, приблизително до титан. И накрая, ако потенциалът на метала е близо до -0,41 V (метали от средната част на серията Zn, Cr, Fe, Ni), тогава, в зависимост от концентрацията на разтвора и условията на електролиза, както редукция на метала, така и отделяне на водород са възможен; често има съвместно освобождаване на метал и водород.
Електрохимичното отделяне на водород от киселинни разтвори възниква в резултат на отделянето на водородни йони. В случай на неутрална или алкална среда, това е резултат от електрохимичната редукция на водата:
2H 2 O + 2e - \u003d H 2 + 2OH -
По този начин естеството на катодния процес по време на електролиза на водни разтвори се определя главно от позицията на съответния метал в поредицата от напрежения. В някои случаи pH на разтвора, концентрацията на метални йони и други условия на електролиза са от голямо значение.
Когато се разглеждат анодни процеси, трябва да се има предвид, че анодният материал може да се окисли по време на електролиза. В тази връзка се разграничават електролиза с инертен анод и електролиза с активен анод. Анодът се нарича инертен, чийто материал не се подлага на окисляване по време на електролиза. Активният анод е анодът, чийто материал може да се окисли по време на електролиза. Като материали за инертни аноди по-често се използват графит, въглища и платина.
На инертен анод по време на електролиза на водни разтвори на алкали, кислородсъдържащи киселини и техните соли, както и флуороводородна киселина и флуориди, протича електрохимично окисление на водата с освобождаване на кислород. В зависимост от pH на разтвора, този процес протича по различен начин и може да се запише в различни уравнения. IN алкална средауравнението изглежда така
4OH - \u003d O 2 + 2H 2 O + 4e -
и в кисела или неутрална:
2H 2 O \u003d O 2 + 4H + + 4e -
В разглежданите случаи електрохимичното окисляване на водата е енергийно най-изгодният процес. Кислородсъдържащите аниони или не могат да се окисляват, или тяхното окисление протича при много високи потенциали. Например, стандартният окислителен потенциал на SO 4 2- йона
2SO 4 2- \u003d S 2 O 8 2- + 2e -
е 2,010 V, което е много по-високо от стандартния потенциал на окисление на водата (1,228 V). Стандартният окислителен потенциал на F йона е още по-голям (2,87 V).
По време на електролизата на водни разтвори на аноксикиселини и техните соли (с изключение на HF и флуориди), анионите се отделят на анода. По-специално, по време на електролиза на разтвори на HI, HBr, HCl и техните соли, съответният халоген се освобождава на анода. Обърнете внимание, че отделянето на хлор по време на електролизата на HCl и неговите соли противоречи на взаимното положение на системите
2Cl - \u003d 2Cl + 2e - (φ \u003d 1,359 V)
2H 2 O \u003d O 2 + 4H + + 4e - (φ \u003d 1,228 V)
в серия от стандартни електродни потенциали. Тази аномалия е свързана със значително пренапрежение на втория от тези два електродни процеса - анодният материал има инхибиторен ефект върху процеса на отделяне на кислород.
В случай на активен анод, броят на конкуриращите се окислителни процеси се увеличава до три: електрохимично окисление на водата с отделяне на кислород, освобождаване на анион (т.е. неговото окисление) и електрохимично окисляване на анодния метал (така нареченото анодно разтваряне на металът). От тези възможни процеси ще протече този, който е енергийно най-благоприятен. Ако анодният метал е разположен в поредица от стандартни потенциали по-рано от двете други електрохимични системи, тогава ще се наблюдава анодно разтваряне на метала. В противен случай ще има отделяне на кислород или анионен разряд.
Нека разгледаме няколко типични случая на електролиза на водни разтвори.
Електролиза на разтвор на CuCl 2 с инертен анод. Медта в поредицата от напрежения се намира след водорода; следователно на катода ще има изхвърляне на Cu 2+ йони и освобождаване на метална мед. В анода ще се изхвърлят хлоридни йони.
Схема на електролиза на разтвор на хлоридна верига (II):
Катод ← Cu 2+ 2Cl - → Анод
Cu 2+ + 2e - \u003d Cu 2Cl - \u003d 2Cl + 2e -
Електролиза на разтвор на K 2 SO 4 с инертен анод. Тъй като калият в поредицата от напрежения е много по-рано от водорода, водородът ще се отдели на катода и OH - ще се натрупа. На анода ще се освободи кислород и ще се натрупат H + йони. В същото време K + йони ще влязат в катодното пространство, а SO 4 2- йони в анодното пространство. Така разтворът във всичките си части ще остане електрически неутрален. Алкалите обаче ще се натрупат в катодното пространство, а киселината ще се натрупа в анодното пространство.
Схема на електролиза на разтвор на калиев сулфат:
Катод ← 4K + 2SO 4 2- → Анод
4H 2 O + 4e - \u003d 4OH - + 4H 2H 2 O \u003d 4H + + 2O + 4e -
KOH 4H \u003d 2H 2 2O \u003d O 2 H 2 SO 4
Електролиза на разтвор на NiSO 4 с никелов анод. Стандартният потенциал на никела (-0,250 V) е малко по-голям от -0,41 V; следователно, по време на електролизата на неутрален разтвор на NiSO 4 върху катода, йоните Ni 2+ се разреждат главно и металът се освобождава. При анода протича обратният процес - окисляването на метала, тъй като потенциалът на никела е много по-малък от потенциала на окисление на водата и още повече от потенциала на окисление на SO 4 2- йона. Така в този случай електролизата се свежда до разтваряне на анодния метал и отделянето му на катода.
Схема за електролиза на разтвор на никелов сулфат:
Катод ← Ni 2+ SO 4 2- → Анод
Ni 2+ + 2e - \u003d Ni Ni \u003d Ni 2+ + 2e -
Този процес се използва за електрохимично пречистване на никел.
Законите на Фарадей
1. Закон на Фарадей.
Масата на веществото, освободено върху електрода при преминаване на електрически ток през електролитния разтвор, е право пропорционална на количеството електричество.
Където ∆m е количеството на реагиралото вещество; Q е количеството електричество; k e - коефициент на пропорционалност, показващ колко вещество е реагирало по време на преминаването на единица електричество. Стойността k се нарича електрохимичен еквивалент.
k=M/(N A z│e│)
където z е валентността на йона; M е моларната маса на веществото, освободено върху електрода; N A е константата на Авогадро. │e│= 1,6 10 -19 Cl.
2. Закон на Фарадей.
Съгласно втория закон на Фарадей, при преминаване на определено количество електричество съотношението на масите на реагиралите вещества е равно на съотношението на техните химични еквиваленти:
∆m 1 /A 1 =∆m 2 /A 2 =∆m 3 /A 3 = const
Химическият еквивалент на елемент е равен на съотношението на частта от масата на елемента, която добавя или замества в химични съединенияедна атомна маса водород или половин атомна маса кислород, до 1/12 от масата на С12 атом. Понятието „химичен еквивалент“ е приложимо и за съединения. По този начин химичният еквивалент на киселина е числено равен на нейната моларна маса, разделена на основността (броя на водородните йони), химическият еквивалент на основата е нейната моларна маса, разделена на киселинността (за неорганична основа, на броя на хидроксилните групи), химичният еквивалент на солта е нейната моларна маса, разделена на сумата от зарядите на катионите или анионите.
Какво представлява електролизата? За по-просто разбиране на отговора на този въпрос, нека си представим всеки източник на постоянен ток. За всеки източник на постоянен ток винаги можете да намерите положителен и отрицателен полюс:
Нека свържем към него две химически устойчиви електропроводими пластини, които ще наречем електроди. Плочата, свързана към положителния полюс, се нарича анод, а към отрицателния полюс се нарича катод:
Натриевият хлорид е електролит; когато се стопи, той се разпада на натриеви катиони и хлоридни йони:
NaCl \u003d Na + + Cl -
Очевидно е, че отрицателно заредените хлорни аниони ще отидат към положително заредения електрод - анода, а положително заредените Na + катиони ще отидат към отрицателно заредения електрод - катода. В резултат на това както Na + катиони, така и Cl - аниони ще бъдат разредени, т.е. те ще станат неутрални атоми. Разрядът възниква чрез придобиване на електрони в случай на Na + йони и загуба на електрони в случай на Cl − йони. Тоест процесът протича на катода:
Na + + 1e − = Na 0 ,
И на анода:
Cl − − 1e − = Cl
Тъй като всеки хлорен атом има несдвоен електрон, тяхното единично съществуване е неблагоприятно и хлорните атоми се комбинират в молекула от два хлорни атома:
Сl∙ + ∙Cl \u003d Cl 2
Така общо процесът, протичащ на анода, е по-правилно написан, както следва:
2Cl - - 2e - = Cl 2
Тоест имаме:
Катод: Na + + 1e − = Na 0
Анод: 2Cl - - 2e - = Cl 2
Нека обобщим електронния баланс:
Na + + 1e − = Na 0 |∙2
2Cl − − 2e − = Cl 2 |∙1<
Добавете лявата и дясната страна на двете уравнения половинчати реакции, получаваме:
2Na + + 2e − + 2Cl − − 2e − = 2Na 0 + Cl 2
Редуцираме два електрона по същия начин, както се прави в алгебрата, получаваме йонното уравнение на електролизата:
2NaCl (л.) => 2Na + Cl 2
От теоретична гледна точка случаят, разгледан по-горе, е най-простият, тъй като в стопилката на натриев хлорид сред положително заредените йони имаше само натриеви йони, а сред отрицателните - само хлорни аниони.
С други думи, нито Na + катиони, нито Cl - аниони са имали "конкуренти" за катода и анода.
А какво ще се случи например, ако вместо стопилка на натриев хлорид се пропусне ток през водния му разтвор? В този случай също се наблюдава дисоциация на натриев хлорид, но образуването на метален натрий във воден разтвор става невъзможно. Все пак знаем, че натрият, представител на алкалните метали, е изключително активен метал, който реагира много бурно с водата. Ако натрият не може да се редуцира при такива условия, тогава какво ще се редуцира на катода?
Нека си припомним структурата на водната молекула. Това е дипол, тоест има отрицателен и положителен полюс:
Благодарение на това свойство той е в състояние да „залепи“ както повърхността на катода, така и повърхността на анода:
Могат да се случат следните процеси:
2H 2 O + 2e - \u003d 2OH - + H 2
2H 2 O - 4e - \u003d O 2 + 4H +
По този начин се оказва, че ако разгледаме разтвор на който и да е електролит, ще видим, че катионите и анионите, образувани по време на дисоциацията на електролита, се конкурират с водните молекули за редукция на катода и окисление на анода.
И така, какви процеси ще протичат на катода и на анода? Изхвърляне на йони, образувани по време на дисоциацията на електролита или окисление / редукция на водни молекули? Или може би всички тези процеси ще се появят едновременно?
В зависимост от вида на електролита, по време на електролизата на неговия воден разтвор са възможни различни ситуации. Например, катиони на алкални, алкалоземни метали, алуминий и магнезий просто не могат да бъдат редуцирани във водната среда, тъй като тяхното редуциране би трябвало да произведе съответно алкални, алкалоземни метали, алуминий или магнезий. метали, които реагират с вода.
В този случай е възможно само намаляването на водните молекули на катода.
Възможно е да запомните какъв процес ще протече на катода по време на електролизата на разтвор на всеки електролит, като следвате следните принципи:
1) Ако електролитът се състои от метален катион, който в свободно състояние в нормални условияреагира с вода, процесът протича на катода:
2H 2 O + 2e - \u003d 2OH - + H 2
Това се отнася за метали, които са в началото на редицата активност на Al, включително.
2) Ако електролитът се състои от метален катион, който в свободната си форма не реагира с вода, но реагира с неокисляващи киселини, протичат два процеса наведнъж, както редукция на метални катиони, така и водни молекули:
Me n+ + ne = Me 0
Тези метали включват тези между Al и H в серията активност.
3) Ако електролитът се състои от водородни катиони (киселина) или метални катиони, които не реагират с неокисляващи киселини, се възстановяват само електролитни катиони:
2H + + 2e - \u003d H 2 - в случай на киселина
Me n + + ne = Me 0 - в случай на сол
Междувременно на анода ситуацията е следната:
1) Ако електролитът съдържа аниони на безкислородни киселинни остатъци (с изключение на F -), тогава процесът на тяхното окисление се извършва на анода, водните молекули не се окисляват. Например:
2Cl - - 2e \u003d Cl 2
S 2- − 2e = S o
Флуорните йони не се окисляват на анода, тъй като флуорът не може да се образува във воден разтвор (реагира с вода)
2) Ако електролитът съдържа хидроксидни йони (алкали), те се окисляват вместо водни молекули:
4OH - - 4e - \u003d 2H 2 O + O 2
3) Ако електролитът съдържа киселинен остатък, съдържащ кислород (с изключение на органични киселинни остатъци) или флуориден йон (F -) на анода, протича процесът на окисляване на водните молекули:
2H 2 O - 4e - \u003d O 2 + 4H +
4) В случай на киселинен остатък от карбоксилна киселина върху анода протича следният процес:
2RCOO - - 2e - \u003d R-R + 2CO 2
Нека се упражним да пишем уравнения за електролиза за различни ситуации:
Пример #1
Напишете уравненията за процесите, протичащи на катода и анода по време на електролиза на стопилка от цинков хлорид, както и общото уравнение на електролизата.
Решение
Когато цинковият хлорид се разтопи, той се дисоциира:
ZnCl 2 \u003d Zn 2+ + 2Cl -
Освен това трябва да се обърне внимание на факта, че стопилката на цинковия хлорид се подлага на електролиза, а не водният разтвор. С други думи, без опции, само редуцирането на цинковите катиони може да се случи на катода и окисляването на хлоридните йони на анода. няма водни молекули
Катод: Zn 2+ + 2e − = Zn 0 |∙1
Анод: 2Cl − − 2e − = Cl 2 |∙1
ZnCl 2 \u003d Zn + Cl 2
Пример #2
Напишете уравненията за процесите, протичащи на катода и анода по време на електролизата на воден разтвор на цинков хлорид, както и общото уравнение на електролизата.
Тъй като в този случай водният разтвор се подлага на електролиза, тогава теоретично водните молекули могат да участват в електролизата. Тъй като цинкът е разположен в серията на активност между Al и H, това означава, че както редукцията на цинковите катиони, така и на водните молекули ще се случи на катода.
2H 2 O + 2e - \u003d 2OH - + H 2
Zn 2+ + 2e − = Zn 0
Хлоридният йон е киселинният остатък на безкислородната киселина HCl, следователно в конкуренцията за окисляване на анода хлоридните йони „печелят“ над водните молекули:
2Cl - - 2e - = Cl 2
В този конкретен случай е невъзможно да се напише общото уравнение на електролизата, тъй като съотношението между водорода и цинка, отделени на катода, е неизвестно.
Пример #3
Напишете уравненията за процесите, протичащи на катода и анода по време на електролизата на воден разтвор на меден нитрат, както и общото уравнение на електролизата.
Медният нитрат в разтвор е в дисоциирано състояние:
Cu(NO 3) 2 \u003d Cu 2+ + 2NO 3 -
Медта е в серията активност вдясно от водорода, тоест медните катиони ще бъдат редуцирани на катода:
Cu 2+ + 2e − = Cu 0
Нитратен йон NO 3 - е киселинен остатък, съдържащ кислород, което означава, че при окисление на анода нитратните йони „губят“ в конкуренцията с водните молекули:
2H 2 O - 4e - \u003d O 2 + 4H +
По този начин:
Катод: Cu 2+ + 2e − = Cu 0 |∙2
2Cu 2+ + 2H 2 O = 2Cu 0 + O 2 + 4H +
Полученото в резултат на добавянето уравнение е йонното уравнение на електролизата. За да получите пълното уравнение на молекулярната електролиза, трябва да добавите 4 нитратни йона към лявата и дясната страна на полученото йонно уравнение като противойони. Тогава ще получим:
2Cu(NO 3) 2 + 2H 2 O = 2Cu 0 + O 2 + 4HNO 3
Пример #4
Напишете уравненията за процесите, протичащи на катода и анода по време на електролизата на воден разтвор на калиев ацетат, както и общото уравнение на електролизата.
Решение:
Калиевият ацетат във воден разтвор се дисоциира на калиеви катиони и ацетатни йони:
CH 3 COOK \u003d CH 3 COO − + K +
Калият е алкален метал, т.е. е в електрохимичната серия от напрежения в самото начало. Това означава, че неговите катиони не могат да се разреждат на катода. Вместо това водните молекули ще бъдат възстановени:
2H 2 O + 2e - \u003d 2OH - + H 2
Както бе споменато по-горе, киселинните остатъци на карбоксилните киселини "печелят" в конкуренцията за окисление от водните молекули на анода:
2CH 3 COO - - 2e - \u003d CH 3 -CH 3 + 2CO 2
По този начин, обобщавайки електронния баланс и добавяйки двете уравнения на полуреакциите на катода и анода, получаваме:
Катод: 2H 2 O + 2e − = 2OH − + H 2 |∙1
Анод: 2CH 3 COO - - 2e - \u003d CH 3 -CH 3 + 2CO 2 | ∙ 1
2H 2 O + 2CH 3 COO - \u003d 2OH - + H 2 + CH 3 -CH 3 + 2CO 2
Получихме пълното уравнение на електролизата в йонна форма. Като добавим два калиеви йона към лявата и дясната страна на уравнението и ги добавим с противойони, получаваме пълното уравнение на електролизата в молекулярна форма:
2H 2 O + 2CH 3 COOK \u003d 2KOH + H 2 + CH 3 -CH 3 + 2CO 2
Пример #5
Напишете уравненията за процесите, протичащи на катода и анода по време на електролизата на воден разтвор на сярна киселина, както и общото уравнение на електролизата.
Сярната киселина се разпада на водородни катиони и сулфатни йони:
H 2 SO 4 \u003d 2H + + SO 4 2-
Водородните катиони H + ще бъдат редуцирани на катода, а водните молекули ще бъдат окислени на анода, тъй като сулфатните йони са киселинни остатъци, съдържащи кислород:
Катод: 2Н + + 2e − = H 2 |∙2
Анод: 2H 2 O - 4e - = O 2 + 4H + |∙1
4H + + 2H 2 O \u003d 2H 2 + O 2 + 4H +
Намалявайки водородните йони в лявата, дясната и лявата страна на уравнението, получаваме уравнението за електролиза на воден разтвор на сярна киселина:
2H 2 O \u003d 2H 2 + O 2
Както се вижда, електролизата на воден разтвор на сярна киселина се свежда до електролиза на вода.
Пример #6
Напишете уравненията за процесите, протичащи на катода и анода по време на електролизата на воден разтвор на натриев хидроксид, както и общото уравнение на електролизата.
Дисоциация на натриев хидроксид:
NaOH = Na + + OH -
Само водните молекули ще бъдат редуцирани на катода, тъй като натрият е силно активен метал, и само хидроксидните йони на анода:
Катод: 2H 2 O + 2e − = 2OH − + H 2 |∙2
Анод: 4OH − − 4e − = O 2 + 2H 2 O |∙1
4H 2 O + 4OH - \u003d 4OH - + 2H 2 + O 2 + 2H 2 O
Нека редуцираме две водни молекули отляво и отдясно и 4 хидроксидни йона и стигнем до извода, че както в случая със сярната киселина, електролизата на воден разтвор на натриев хидроксид се свежда до електролиза на вода.










